
某原电池装置如图所示,电池总反应为2Ag+Cl2===2AgCl。下列说法正确的是( )
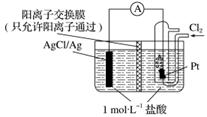
A.正极反应为AgCl+e-===Ag+Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
科目:高中化学 来源: 题型:
下列有关原电池的说法中正确的是( )
A.在外电路中,电子由负极流向正极
B.在原电池中,相对较活泼的金属作负极,不活泼的金属作正极
C.原电池工作时,正极表面一定有气泡产生
D.原电池工作时,可能会伴随着热能变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是一种航天器能量储存系统原理示意图。下列说法正确的是( )

A.该系统中只存在3种形式的能量转化
B.装置Y中负极的电极反应式为:O2+2H2O+4e-===4OH-
C.装置X能实现燃料电池的燃料和氧化剂再生
D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化
查看答案和解析>>
科目:高中化学 来源: 题型:
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是( )
A.由Al、Cu、稀H2SO4组成的原电池,负极反应式为Al-3e-===Al3+
B.由Mg、Al、NaOH溶液组成的原电池,负极反应式为Al-3e-+4OH-===AlO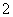 +2H2O
+2H2O
C.由Fe、Cu、FeCl3溶液组成的原电池,负极反应式为Cu-2e-===Cu2+
D.由Al、Cu、浓硝酸组成的原电池,负极反应式为Cu-2e-===Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
银制器皿表面日久因生成Ag2S而变黑,可进行如下处理:将表面发黑的银器浸入盛有食盐水的铝质容器中(如图),一段时间后黑色褪去。有关说法正确的是( )
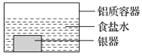
A.该处理过程中电能转化为化学能
B.银器为正极,Ag2S还原为单质银
C.Ag2S溶解于食盐水生成了AgCl
D.铝质容器为阳极,其质量变轻
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M和N均为短周期元素,X、Y、Z原子序数依次增大且最外层电子数之和为15,X与Z可形成XZ、XZ2型分子, Y与M气态化合物标准状况下密度约0.76g/L。N的原子半径为短周期元素中最大。回答下列问题:
(1)M、Z和N的元素符号分别为 、 、 。
(2)X、Y、Z、M四种元素的原子半径由大到小的顺序为 。
(3)由上述元素组成、既含有共价键又含有离子键的化合物,其中含有极性共价键或含有非极性共价键,各举一例用电子式表示为 、 。
(4)X和Y组成的离子XY-对环境有害,可在NaClO的碱性溶液中转化为碳酸盐和氮气,相应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
构成物质的微粒种类及相互间的作用力是决定物质表现出何种物理性质的主要因素。
(1)三氯化铁常温下为固体,熔点282 ℃,沸点315 ℃,在300 ℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体中存在的微粒间作用力有_____________________________________________________________。
(2)氢键作用常表示为“A—H…B”,其中A、B为电负性很强的一类原子,如_____________________________________________________(列举三种)。
X、Y两种物质的分子结构和部分物理性质如下表,两者物理性质有差异的主要原因是_________________________________________________________________________________________________________________________________。
| 代号 | 结构简式 | 水中溶解 度/g(25 ℃) | 熔点/ ℃ | 沸点/ ℃ |
| X |
| 0.2 | 45 | 100 |
| Y |
| 1.7 | 114 | 295 |
(3)钙是人体所需的重要元素之一,有一种补钙剂——抗坏血酸钙的组成为Ca(C6H7O6)2·4H2O,其结构示意图如下:
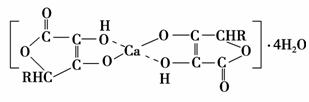
该物质中存在的化学键类型包括________(填字母)。
A.极性共价键 B.离子键
C.非极性共价键 D.配位键
(4)①CH2===CH2、②CH≡CH、③ 、④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是________。这四种分子中碳原子采取sp2杂化的是________(填序号)。
、④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是________。这四种分子中碳原子采取sp2杂化的是________(填序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com