
| A. | 0.1mol•L-1 FeCl3溶液:K+、NH${\;}_{4}^{+}$、I-、SCN- | |
| B. | 使甲基橙试液呈红色的溶液:K+、Na+、SO${\;}_{4}^{2-}$、AlO${\;}_{2}^{-}$ | |
| C. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13 mol•L-1的溶液中:Al3+、Ca2+、Cl-、NO${\;}_{3}^{-}$ | |
| D. | 水电离产生的c(OH-)=10-12 mol•L-1的溶液:NH${\;}_{4}^{+}$、Mg2+、HCO${\;}_{3}^{-}$、Cl- |
分析 A.铁离子能够与碘离子、硫氰根离子反应;
B.使甲基橙试液呈红色的溶液呈酸性,偏铝酸根离子与酸性溶液中的氢离子反应;
C.该溶液中存在大量氢离子,四种离子之间不反应,都不与氢离子反应;
D.水电离产生的c(OH-)=10-12 mol•L-1的溶液呈酸性或碱性,碳酸氢根离子与氢离子、氢氧根离子反应.
解答 解:A.FeCl3溶液的铁离子能够与I-、SCN-发生反应,在溶液中不能大量共存,故A错误;
B.使甲基橙试液呈红色的溶液中存在大量氢离子,AlO2-与氢离子反应,在溶液中不能大量共存,故B错误;
C.该溶液呈酸性,溶液中存在大量氢离子,Al3+、Ca2+、Cl-、NO3-之间不反应,都不与氢离子反应,在溶液中能够大量共存,故C正确;
D.水电离产生的c(OH-)=10-12 mol•L-1的溶液中存在大量氢离子或氢氧根离子,Mg2+、NH4+、HCO3-与氢氧根离子反应,HCO3-与氢离子反应,在溶液中一定不能大量共存,故D错误;
故选C.
点评 本题考查离子共存,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:选择题
| A. | 硅酸是一种很弱的酸 | |
| B. | 硅酸可由二氧化硅与水反应制得 | |
| C. | 硅酸不稳定,加热脱水会生成二氧化硅 | |
| D. | 硅酸可以由可溶性硅酸盐与盐酸反应制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Cl->F->Na+>Al3+ | B. | 非金属性:Cl>S>P>Si | ||
| C. | 酸性:H2SiO3>H2CO3>H3PO4 | D. | 热稳定性:PH3<H2S<HCl<HF |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
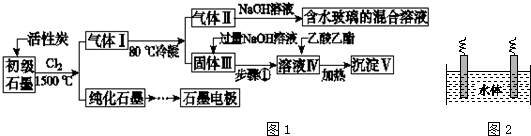
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL质量分数为98%的H2O4,用水稀释至100mL,H2SO4的质量分数为9.8% | |
| B. | 在H2O2+Cl=2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 | |
| C. | 标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g | |
| D. | 密闭容器中2mo1NO与1moIO2充分反应,产物的分子数小于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,pH均为9的CH3COONa和NaOH溶液中,水的电离程度相同 | |
| B. | 室温下,0.1mol•L-1氨水加水稀释后,溶液中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$的值减小 | |
| C. | 电解精炼铜过程中,阳极减少的质量与阴极增加的质量一定相等 | |
| D. | 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,则该反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔 | B. | 丙烯 | C. | 丙炔 | D. | 1,3-丁二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Pb为正极被氧化 | B. | SO42-只向PbO2极移动 | ||
| C. | 电解质溶液密度不断减小 | D. | 电解质溶液浓度不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com