
 ,该物质可由下列哪组物质为原料直接合成得到( )
,该物质可由下列哪组物质为原料直接合成得到( )A、 和CH3CH2OH 和CH3CH2OH |
B、 和HOCH2CH2OH 和HOCH2CH2OH |
C、 和CH3CH2OH 和CH3CH2OH |
D、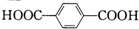 和HOCH2CH2OH 和HOCH2CH2OH |
 的结构简式可知,该高分子化合物为缩聚反应产物,将中括号去掉,将酯基按照酯的水解原理断开,然后在含有碳氧双键的一端添上羟基,在氧原子一端添上氢原子,可得该高分子化合物的单体:
的结构简式可知,该高分子化合物为缩聚反应产物,将中括号去掉,将酯基按照酯的水解原理断开,然后在含有碳氧双键的一端添上羟基,在氧原子一端添上氢原子,可得该高分子化合物的单体: 和HOCH2CH2OH,
和HOCH2CH2OH,

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ⅦA族元素 | B、聚乙烯 |
| C、ⅠA族元素 | D、二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、催化剂的使用可实现SO2的转化率为100% |
| B、达到化学平衡时,各物质的浓度不再改变 |
| C、其他条件不变,升高温度,不能增大反应的速率 |
| D、其他条件不变,降低SO3的浓度,可以增大反应的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3-CH2-CH3和CH3-CH2-CH2-CH3 |
B、CH3一CH=CH-CH3和 |
| C、CH3-CH=CH-CH3和CH3-CH2-CH=CH2 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ||||||||
| ② | ③ | ④ | ⑤ | |||||
| ⑥ | ⑦ | ⑧ | ⑨ | |||||
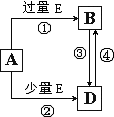
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 300 | 400 | 500 | 750 | 1000 |
| 平衡常数 | 1.8 | 1.6 | 1.0 | 0.8 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com