
| A. | 土壤胶体带负电荷,有利于铵态氮肥的吸收 | |
| B. | “辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 | |
| C. | SiCl4在战争中常用作烟雾弹,是因为它水解时生成白色烟雾 | |
| D. | “雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物无关 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | A与C形成的化合物溶于水所得溶液显碱性 | |
| B. | B与D形成的化合物溶于水所得溶液显酸性 | |
| C. | 氢化物的稳定性:C>D | |
| D. | 简单离子的半径:B>C>D>A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应速率与Ag+浓度有关 | B. | Ag2+也是该反应的催化剂 | ||
| C. | Ag+能降低该反应的活化能和焓变 | D. | v(Cr3+)=v(S2O82-) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加KSCN溶液 | 溶液变红色 | 固体物质中有FeCl3 |
| 在酸性KMnO4溶液中加少量A溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含FeCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
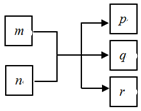 短周期元素W、X、Y、Z的原子序数依次增大,且分布在三个不同的周期里.Y元素的焰色为黄色.由上述元素组成的物质之间的转化关系如图(反应条件略去),其中m、n、p化合物,q、r是单质,r通常为黄绿色气体,常温下0.01mol•L-1 p溶液的pH为12.下列说法不正确的是( )
短周期元素W、X、Y、Z的原子序数依次增大,且分布在三个不同的周期里.Y元素的焰色为黄色.由上述元素组成的物质之间的转化关系如图(反应条件略去),其中m、n、p化合物,q、r是单质,r通常为黄绿色气体,常温下0.01mol•L-1 p溶液的pH为12.下列说法不正确的是( )| A. | 简单离子半径的大小:Y<X<Z | |
| B. | X的简单氢化物的沸点在同族元素中最高 | |
| C. | Y分别与W、Z形成的两种化合物中化学键类型相同 | |
| D. | Z的氧化物对应的水化物为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
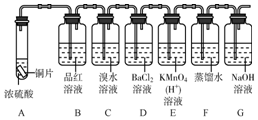 下面是某同学学习硫元素的学习方案.
下面是某同学学习硫元素的学习方案.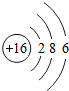 ,从结构知道硫元素是一种典型非金属元素.
,从结构知道硫元素是一种典型非金属元素.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HF<HCl<HBr<HI | B. | 微粒半径:K+>Na+>Mg2+>Al3+ | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 最外层电子数Li<Mg<Si<Ar |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “滴水石穿,绳锯木断”不包含化学变化 | |
| B. | “天宫一号”中使用的碳纤维,是一种新型有机高分子材料 | |
| C. | 二氧化硅可用于光纤通信、单晶硅可用于光电转换 | |
| D. | 淀粉、油脂和蛋白质都是高分子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com