
【题目】一定条件下,反应室(容积恒定为2 L)中有反应:A(g)+2B(g)=C(g)。
(1)能说明上述反应达到平衡状态的是________(填字母,下同)。
A.反应中A与B的物质的量浓度之比为1∶2
B.混合气体总物质的量不再变化
C.混合气体的密度不随时间的变化而变化
D.2v正(A)=v逆(B)
(2)1 mol A(g)与2 mol B(g)在催化剂作用下在反应室反应生成C(g),A的平衡转化率与温度、压强的关系如图所示:

①p1________(填“<”、“>”或“=”,下同)p2,正反应的ΔH________0。
②下列措施中一定能使c(C)/c(A)增大的是________。
A.升高温度 B.恒温恒容再充入A
C.恒温恒容再充入B D.恒温恒容再充入1 mol C
(3)100 ℃时将1 mol A和2 mol B通入反应室,保持温度不变,10 min末C(g)的浓度为0.05 mol·L-1,则10 min末B的转化率为________,此时v正_______v逆(填“<”、“>”或“=”)。
【答案】BD < < CD 10% >
【解析】
(1)根据化学平衡状态的特征此解答该题;
(2)根据温度和压强对化学平衡移动的影响因素来判断;能使c(C)/c(A)增大的因素即能使化学平衡正向移动即可;
(3)根据三行式计算化学反应的转化率,结合Qc和K的关系判断化学反应的方向。
(1)A.反应中A与B的物质的量浓度之比为1:2,不一定达到化学平衡状态,故A错误;
B.反应前后气体系数和不相等,混合气体总物质的量不再变化,达到了平衡状态,故B正确;
C.混合气体的密度=m/V,气体总质量是不变的,体积不变,密度始终不随时间的变化而变化,故C错误;
D.2v正(A)=v逆(B),证明正逆反应速率是相等的,故D正确;
答案:BD
(2)①根据图中信息知道,温度升高,A的转化率减小,化学平衡逆向移动,所以反应是放热反应,焓变小于零;温度不变,压强越大,A的转化率越大,所以P1<P2;
答案:< <
②A.升高温度,平衡逆向移动,所以比值减小,故A错误;
B.恒温恒容再充入A,分子分母均增大,但是分母增加的程度大,所以比值减小,故B错误;
C.恒温恒容再充入B,平衡正向移动,所以比值增大,故C正确;
D.恒温恒容再充入1molC,相当于增大压强,平衡逆向移动,比值增大,故D正确;
答案:CD
(4)设B的变化量是x,则
A(g)+ 2B(g)![]() C(g)
C(g)
初始浓度: 0.5 1 0
变化浓度1: 0.5x x 0.5x
末态浓度:0.5-0.5x 1-x 0.5x
变化浓度2: 0.25 0.5 0.25
平衡浓度: 0.25 0.5 0.25
10min末C(g)的浓度为0.05mol/L,即此时0.5x=0.05,所以x=0.1,所以B的转化率是0.1/1×100%=10%,此时Qc=![]() ≈0.14;K=
≈0.14;K=![]() =4,所以Qc<K,化学平衡正向移动,即正反应速率大于逆反应速率;答案:10% >。
=4,所以Qc<K,化学平衡正向移动,即正反应速率大于逆反应速率;答案:10% >。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】25℃条件下,向![]() 的盐酸中不断通
的盐酸中不断通![]() ,该过程中水电离出的氢离子浓度
,该过程中水电离出的氢离子浓度![]() 水
水![]() 与通入
与通入![]() 的物质的量关系如图,下列说法不正确的是( )。
的物质的量关系如图,下列说法不正确的是( )。
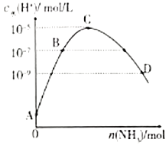
A.![]() 点的纵坐标为
点的纵坐标为![]()
B.![]() 点溶液中
点溶液中![]()
C.![]() 点溶液中
点溶液中![]()
D.![]() 点溶液的
点溶液的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,又可作为燃料,工业上可利用CO或CO2来生产燃料甲醇。已知制备甲醇的有关反应的化学方程式及其在不同温度下的化学平衡常数如表所示。
化学反应 | 化学平衡常数 | 温度(℃) | ||
500 | 700 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.34 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 1.70 | 2.52 |
③3H2(g)+CO2(g) | K3 | |||
(1)下列措施能使反应③的平衡体系中![]() 增大的是__
增大的是__
A.将H2O(g)从体系中分离出去 B.恒容时充入He(g),使体系压强增大
C.升高温度 D.恒容时再充入1molH2(g)
(2)T℃时,反应③在恒容密闭容器中充入1molCO2和nmolH2,混合气体中CH3OH的体积分数与氢气的物质的量的关系如图1所示。图1中A、B、C三点对应的体系,CO2的转化率最大的是___(填字母)。
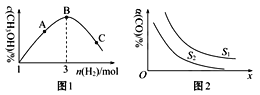
(3)工业上也用合成气(H2和CO)合成甲醇,反应为2H2(g)+CO(g)![]() CH3OH(g) ΔH<0,在10L的恒容密闭容器中充入H2和C物质的量比为2:1,测得CO的平衡转化率与温度、压强的关系如图2所示。
CH3OH(g) ΔH<0,在10L的恒容密闭容器中充入H2和C物质的量比为2:1,测得CO的平衡转化率与温度、压强的关系如图2所示。
①图2中S代表的物理量是___。
②300℃时,氢气的物质的量随时间变化如表所示
反应时间/min | 0 | 1 | 4 | 5 |
H2/mol | 8 | 5.4 | 4 | 4 |
在该温度下,上述反应的平衡常数为___。若再向该平衡体系中再加入2molCO、2molH2、2molCH3OH,保持温度和容器体积不变,则平衡会___(填“正向移动”“逆向移动”或“不移动”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是

选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如下图所示。
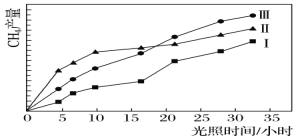
(1)在0~30小时内,CH4的平均生成速率vⅠ、vⅡ、vⅢ从大到小的顺序为__________;反应开始后的12小时内,在第________种催化剂作用下,收集的CH4最多。
(2)将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206 kJ·mol-1。
①在下列坐标图中,画出反应过程中体系能量变化图(进行必要标注)。________;

②将等物质的量的CH4和H2O(g)充入1 L恒容密闭反应器,某温度下反应达平衡,平衡常数K=27,此时测得CO的物质的量为0.10 mol,则CH4的平衡转化率为________(结果保留两位有效数字)。
(3)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-802 kJ·mol-1,写出由CO2生成CO的热化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下的一密闭容器中事先放入1.56g过氧化钠,然后再通入乙烷与氧气的混合气体,用电火花引爆,直至反应完全为止,恢复到原温度,容器内压强近似为零。
(1)相同条件下,通入的气体氧气和乙烷的体积比是多少?_____
(2)通入氧气的质量最大应是多少?_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计了一种太阳能驱动从海水中提取金属锂的装置,示意图如图所示。该装置工作时,下列说法正确的是

A.铜箔上的电势比催化电极上的高
B.海水的pH变大
C.若转移1mol电子,理论上铜箔增重7g
D.固体陶瓷膜可用质子交换膜代替
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2(g)![]() 2NO(g)+O2(g)在密闭容器中反应,达到平衡状态的标志是
2NO(g)+O2(g)在密闭容器中反应,达到平衡状态的标志是
A.单位时间内生成n molO2的同时,生成2nmolNO
B.用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
C.混合气体的质量不再改变的状态
D.混合气体的平均相对分子质量不再改变的状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,40 g、10%硝酸钠溶液与60 g、7.5%的硝酸钠溶液混合,得到密度为1.20 g·cm-3的混合溶液,计算:
(1)该混合溶液中溶质的质量分数为__;
(2)该混合溶液中NaNO3的物质的量浓度为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com