
下列物质的金属键最强的是( )
A.Na B.Mg
C.K D.Ca
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
| 化学键 | Si—O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”)。
SiC________Si;SiCl4________SiO2。
(2)下图立方体中心的“●”表示硅晶体中的一个原子,请在立方体的顶点用“●”表示出与之紧邻的硅原子。
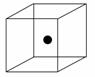
(3)工业上高纯硅可通过下列反应制取:
SiCl4(g)+2H2(g)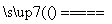 Si(s)+4HCl(g)
Si(s)+4HCl(g)
该反应的反应热ΔH=________kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列指定微粒的个数比为2∶1的是( )
A.Be2+离子中的质子和电子
B.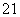 H原子中的中子和质子
H原子中的中子和质子
C.NaHCO3晶体中的阳离子和阴离子
D.BaO2(过氧化钡)固体中的阴离子和阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
金属键的形成是通过( )
A.金属原子与自由电子之间的相互作用
B.金属离子与自由电子之间强烈的相互作用
C.自由电子之间的相互作用
D.金属离子之间的相互作用
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于晶体的性质叙述中,不正确的是( )
A.晶体的自范性指的是在适宜条件下晶体能够自发地呈现封闭规则的多面体几何外形
B.晶体的各向异性和对称性是矛盾的
C.晶体的对称性是微观粒子按一定规律做周期性重复排列的必然结果
D.晶体的各向异性直接取决于微观粒子的排列具有特定的方向性
查看答案和解析>>
科目:高中化学 来源: 题型:
金属晶体中金属原子有三种常见的堆积方式:六方堆积、面心立方堆积和体心立方堆积。a、b、c分别代表这三种晶胞的结构,其晶胞a、b、c内金属原子个数比为( )
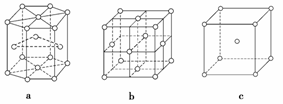
A.3∶2∶1 B.11∶8∶4
C.9∶8∶4 D.21∶14∶9
查看答案和解析>>
科目:高中化学 来源: 题型:
据某科学杂志报道,国外有一研究机构发现了一种新的球形分子,它的分子式为C60Si60,其分子结构酷似中国传统工艺“镂雕”,经测定其中包含C60,并且也有Si60结构,下列叙述不正确的是( )
A.该物质有很高的熔点,很大的硬度
B.该物质形成的晶体属于分子晶体
C.该物质分子中C60被包裹在Si60里面
D.该物质的相对分子质量为2 400
查看答案和解析>>
科目:高中化学 来源: 题型:
普通玻璃和水晶的根本区别在于( )
A.外形不一样
B.普通玻璃的基本构成微粒无规则性地排列,水晶的基本构成微粒按一定规律做周期性重复排列
C.水晶有固定的熔点,普通玻璃无固定的熔点
D.水晶可用于能量转换,普通玻璃不能用于能量转换
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com