
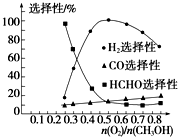
| n(O2) |
| n(CH3OH) |
| n(O2) |
| n(CH3OH) |
| ������ƽ��Ũ���ݴη��˻� |
| ��Ӧ��ƽ��Ũ���ݴη��˻� |
| ���� |
| һ���¶� |
| n(O2) |
| n(CH3OH) |
| ������ƽ��Ũ���ݴη��˻� |
| ��Ӧ��ƽ��Ũ���ݴη��˻� |
| ||||
|
| 4 |
| 3 |
| 4 |
| 3 |
| ���� |
| һ���¶� |
| n(O2) |
| n(CH3OH) |
| n(O2) |
| n(CH3OH) |
| ���� |
| һ���¶� |


 Ʒѧ˫�ž�ϵ�д�
Ʒѧ˫�ž�ϵ�д� Сѧ��ĩ���100��ϵ�д�
Сѧ��ĩ���100��ϵ�д� ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������̼ԭ������Ϊ1��1 |
| B�������Ϊ11��7 |
| C���ܶȱ�Ϊ7��11 |
| D����������Ϊ7��11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
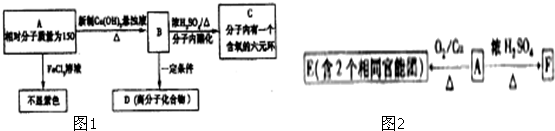
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
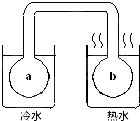 ��ͼ��ʾ���ܷ�˫����ϵ�г��к���ɫ����X���������ձ���ˮԡ����²����a��������ɫ��b���������ɫ�����������Һ��������X�����ǣ�������
��ͼ��ʾ���ܷ�˫����ϵ�г��к���ɫ����X���������ձ���ˮԡ����²����a��������ɫ��b���������ɫ�����������Һ��������X�����ǣ�������| A��NO2��g�� |
| B��Br2��g�� |
| C��NO��g�� |
| D��N2��g�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��11.2LH2��0.5molCO2 |
| B��18mLH2O��4�棩��2��105Pa��27��32gO2 |
| C��1molCO��88gCO2 |
| D��27�棬22.4LCl2�ͺ�4mol��ԭ�ӵ�H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڱ�״���£�11.2L ��������NA����ԭ�� |
| B��25�棬1.01��105Pa��64gSO2�к��е�ԭ����Ϊ3NA |
| C��11.2L CO���еķ�����Ϊ0.5NA |
| D��1mol�����Ӻ��еĵ�������1mol�������еĵ�����֮��Ϊ16��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��Ʒ�� | GB5461 |
| ��Ʒ�ȼ� | һ�� |
| �� �� | ʳ�Ρ�����ء������ |
| �⺬������I�ƣ� | 20��50mg/kg |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�� װ�� |  |  |  |  |
| ����ʵ ������ | a��������С��b���������� | b�������������c���ޱ仯 | d���ܽ⣬c����������� | ������a������d�� |
| A��a��b��c��d |
| B��b��c��d��a |
| C��d��a��b��c |
| D��a��b��d��c |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com