
(16分)污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。

请回答下列问题:
(1)上述流程中多次涉及到过滤操作,实验室进行过滤操作时需要用到的硅酸盐仪器有玻璃棒、 、 ;其中玻璃棒的作用是 。
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原理是 。
(3)已知Ksp(CuS)=8.4×10-45,Ksp(NiS)=1.4×10-24;在除铜镍的过程中,当Ni2+恰好完全沉淀 (此时溶液中c(Ni2+)=1.0×10-5mol/L),溶液中Cu2+的浓度是 mol/L。
(4)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中隋性电极作阳极,铁作阴极,请写出阳极的电极反应式 。
(5)下列各组试剂中,能准确测定一定体积燃煤尾气中SO2含量的是__________。(填编号)
a.NaOH溶液、酚酞试液
b.稀H2SO4酸化的KMnO4溶液
c.碘水、淀粉溶液
d.氨水、酚酞试液
(6)除杂后得到的MnSO4溶液可以通过 (填操作名称)制得硫酸锰晶体(MnSO4?H2O,相对分子质量为169)。已知废气中SO2浓度为8.4 g/m3,软锰矿浆对SO2的吸收率可达90%,则处理1000 m3燃煤尾气,可得到硫酸锰晶体质量为 kg(结果保留3位有效数字)。
(16分)(1)烧杯 漏斗(各1分,共2分);引流,防止液体溅出。(2分)
(2)消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀(2分)
(3)6.0×10-26mol/L(2分)
(4)MnO42-—e-= MnO4- (2分)
(5)b c (2分)
(6)蒸发浓缩,冷却结晶(过滤),(2分) 20.0(2分)
【解析】
试题分析:(1)过滤操作需要烧杯、漏斗、玻璃棒,这三种玻璃仪器都是硅酸盐仪器;其中玻璃棒是作用是引流,防止液体溅出的作用;
(2)铝离子与铁离子水解产生氢氧化铝、氢氧化铁和氢离子,加入MnCO3能消耗水解平衡的氢离子,使平衡正向移动,从而使Al、Fe沉淀被除去;
(3)当Ni2+恰好完全沉淀 (此时溶液中c(Ni2+)=1.0×10-5mol/L),溶液中S2-的浓度根据,Ksp(NiS)=1.4×10-24可得c(S2-)=1.4×10-24/1.0×10-5=1.4×10-19mol/L,则根据Ksp(CuS)=8.4×10-45,可得溶液中Cu2+的浓度是8.4×10-45/1.4×10-19=6.0×10-26mol/L;
(4)电解池中阳极发生氧化反应,元素的化合价升高,则MnO42-被氧化为MnO4-,所以阳极的电极反应式为MnO42-—e-= MnO4-;
(5)a、二氧化硫与氢氧化钠溶液反应,生成的亚硫酸钠或亚硫酸氢钠或二者的混合物,产物的量无法确定,所以不能计算二氧化硫的含量,错误;b、二氧化硫与酸性高锰酸钾溶液发生氧化还原反应,反应只有一步,产物固定,所以可以准确计算二氧化硫的含量,正确;c、二氧化硫与淀粉、碘水溶液发生氧化还原反应,产物固定,且现象明显,可以准确计算二氧化硫的含量,正确;d、氨水是弱碱溶液,与二氧化硫反应的产物可能是亚硫酸铵、亚硫酸氢铵、或者二者的混合物,产物不固定,所以不能准确计算二氧化硫的含量,错误,答案选bc;
(6)从溶液中得到晶体的操作是蒸发浓缩、冷却结晶,过滤可得硫酸锰晶体;1000 m3燃煤尾气中二氧化硫的物质的量是1000 m3×8.4 g/m3/64g/mol,二氧化硫的吸收率是90%,根据S元素守恒,则可得到硫酸锰晶体的质量是1000 m3×8.4 g/m3/64g/mol×90%×169g/mol=20.0kg。
考点:考查实验基本操作的判断,仪器的选择,对流程的分析,溶度积常数的应用,实验方案的评价,实验结果的分析与计算


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年四川省德阳市高三一诊考试化学试卷(解析版) 题型:填空题
(16分)X、Y、Z、E、M、Q、R为七种短周期的主族元素,它们的原子序数依次增大,其中X+无电子,Y、Z同一周期且相邻,X与E、Z与Q分别为同一主族,M的原子序数是Y的2倍,Q的质子数比E多5。J为ds区原子序数最小的元素。请用推断出的元素回答下列问题:
(1)Y、Z、Q三元素的第一电离能由大到小的顺序为__________,Y2 、X2分子中共价键的数目之比为_________,MR4分子的中心原子的杂化轨道类型是_______。
(2)由Q、R两元素可按原子个数比l:l组成化合物T,化合物T中各原子均满足8电子的稳定结构,则T的电子式为________。固体化合物E2Z2投人到化合物E2Q的水溶液中,只观察到有沉淀产生,该反应的离子方程式为______________________。
(3)J元素基态原子的外围电子排布式为___________。向JQZ4溶液中逐滴加人Y元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解得到深蓝色的透明溶液,该沉淀溶解的离子方程式是_____________。
(4)J2Z为半导体材料,在其立方晶胞内部有4个Z原子,其余Z原子位于面心和顶点,则该晶胞中有______个J原子。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高密市高三12月检测理综化学试卷(解析版) 题型:选择题
某硫酸厂废气中SO2的回收利用方案如右下图所示。下列说法不正确的是
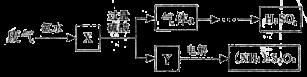
A.X可能含有2种盐 B.a是SO3
C.Y可能含有(NH4)2SO4 D.(NH4)2S2O8中S的化合价可能为+7
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省英文学校高三上学期12月月考化学试卷(解析版) 题型:选择题
利用图中所示装置进行下列实验,能得出相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓盐酸 | MnO2 | NaOH | 制氯气并吸收尾气 | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省英文学校高三上学期12月月考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3+ + 2I- = 2Fe2+ + I2
B、氧化铝溶解在NaOH溶液中:3H2O + Al2O3 + 2OH-?= 2[Al(OH)4]-?
C、硫酸铝溶液与氢氧化钡溶液反应,使SO42-恰好沉淀完全Al3+ + SO42-?+ Ba2+ + 3OH- = BaSO4 ↓ + Al(OH)3↓
D、在漂白粉配制成的溶液中通入SO2:Ca2+ + 2ClO- + SO2 + H2O = CaSO3↓+ 2HClO
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省六校联盟高三第三次联考理科综合试卷(解析版) 题型:选择题
50℃时,0.1mol·L-1Na2CO3溶液pH=12,下列判断正确的是
A.c(OH-)=10-2mol·L-1
B.加入少量NaOH固体,c(Na+)和c(CO32-)均增大
C.c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
D.2c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期12月月考化学试卷(解析版) 题型:填空题
(10分)榴石矿石可以看作由CaO、FeO、Fe2O3、Al2O3、SiO2组成。工业上对其进行综合利用的流程如下:
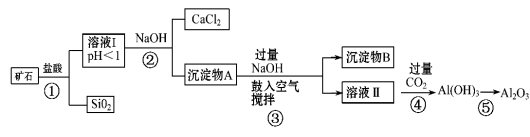
(1)SiO2的用途广泛,试写出其中的一种重要用途 ;
(2)溶液Ⅰ中除了Ca2+外,还含有的金属阳离子有 ;
(3)步骤③中NaOH参加反应的离子方程式是 ,
鼓入空气并充分搅拌的目的是(用化学方程式表示): 。
(4)在工业生产中,步骤④通入过量CO2而不加入盐酸的原因是 ________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期12月月考化学试卷(解析版) 题型:选择题
现有一瓶乙二醇和丙三醇的混合物,已知它们的性质如下表,据此,将乙二醇和丙三醇互相分离的最佳方法是
物质 | 分子式 | 熔点(℃) | 沸点(℃) | 密度 | 溶解性 |
乙二醇 | C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | C3H8O3 | 17.9 | 290 | 1.26 | 能跟水和酒精以任意比互溶 |
A.萃取法 B.结晶法 C.分液法 D.蒸馏法
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一12月月考化学试卷(解析版) 题型:选择题
将一小块钠投入下列溶液中,既能产生气体又会出现白色沉淀的是
A.稀H2SO4 B.氢氧化钠溶液 C.硫酸铜溶液 D.氯化镁溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com