
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2017届广东省高三上学期期中化学试卷(解析版) 题型:填空题
太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、锎、硼、镓、硒等。回答下列问題:
⑴二价铜离子的电子排布式为 ,已知高温下Cu2O比CuO更稳定,试从铜原子核外电子结构变化角度解释 。

⑵如图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 。
⑶往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是 。
⑷铜与类卤素(SCN)2反应生成Cu(SCN)2,1mol(SCN)2中含有π键的数目为 ,类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H—S—C≡N)的沸点低于异硫氰酸(H—N=C=S)的沸点。其原因是 。
⑸硼元素具有缺电子性,其化合物可与具有孤电子对的分子或离子形成配合物,如BF3能与NH3反应生成BF3•NH3,在BF3•NH3中B原子的杂化方式为 ,B与N之间形成配位键,氮原子提供 。
⑹六方氮化硼晶体结构与石墨晶体相似,层间相互作用为 。六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构和硬度都与金刚石相似,晶胞结构如下图所示,晶胞边长为361.5pm,立方氮化硼的密度是 g/cm3。(只要求列算式)。

查看答案和解析>>
科目:高中化学 来源:2016-2017黑龙江牡丹江第一高级中学高二上期末化学卷(解析版) 题型:选择题
下列说法正确是
A.糖类、油脂、蛋白质完全燃烧只生成CO2和H2O
B.丁烷(C4H10)和二氯甲烷都存在同分异构体
C.向溴水中加入苯,振荡静置后观察下层几乎无色
D.汽油、柴油、植物油都是碳氢化合物
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二12月月考化学卷(解析版) 题型:选择题
下列溶液中c(Cl—)与150mL 1mol/L NaCl溶液中c(Cl—)相等的是
A.50mL 3mol/L KCl溶液 B.75 mL 2mol/L CaCl2溶液
C.100 mL 0.5mol/L BaCl2溶液 D.50mL 1mol/L AlCl3溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二12月月考化学卷(解析版) 题型:选择题
化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是( )
A.棉花和木材的主要成分都是纤维素、蚕丝和人造丝的主要成分都是蛋白质
B.腌制熟食品时,添加少量亚硝酸钠,是为了使其味道更加美味可口
C.为了防止月饼等富脂食品氧化变质,延长食品的保质期,常在包装袋中放入生石灰
D.“神七”宇航员所穿出舱航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成的,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它 是一种新型无机非金属材料
是一种新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二12月月考化学卷(解析版) 题型:选择题
下列有关城市各项污染源与其造成的恶果对应正确的是( )
A.汽车尾气——光化学烟雾 工业废气——酸雨 工业废水——“公害病”
B.汽车尾气——酸雨 工业废气——“公害病” 工业废水——光化学烟雾
C.汽车尾气——“公害病” 工业废气——酸雨 工业废水——光化学烟雾
D.汽车尾气——光化学烟雾 工业废气——“公害病” 工业废水——酸雨
查看答案和解析>>
科目:高中化学 来源:2017届浙江省“七彩阳光”新高考研究联盟高三上考试化学试卷(解析版) 题型:实验题
工业上湿法制高铁酸钾的基本流程如下:
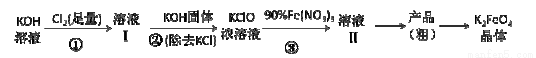
已知:高铁酸盐热稳定性差
回答下列问题:
(1)第③步发生反应的离子方程式 。
(2)第③步反应的体系,温度不宜过高,并最好控制温度在 30℃以下,其原因是 。
(3)通过结晶方法从溶液II得到的粗产品中主要含有杂质 (填化学式),可通过重结晶法提纯K2FeO4,具体操作步骤有:将粗产品先用饱和KOH溶液溶解,然后浓缩、冷却结晶、过滤、洗涤、干燥。其干燥可采用的方法是 (写出一种干燥方法)。
(4)利用电化学原理,用铁钉和氢氧化钾溶液为原料可以获得K2FeO4。在制备过程中铁钉作______极,请写出获得FeO42-的电极反应式 。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省“七彩阳光”新高考研究联盟高三上考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 质子数相同的微粒一定属于同一种元素
B. 质子数相同,电子数也相同的两种微粒,可以是一种分子和一种离子。
C. 质量数在数值上等于该元素原子的相对原子质量取整数。
D. 同种元素的不同核素互称为同素异形体
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江哈尔滨六中高三上学期期末化学卷(解析版) 题型:实验题
过氧化钙是一种重要的化工原料,温度在350℃以上容易分解。
(1)利用反应Ca(s)+O2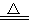 CaO2(s),在纯氧条件下,制取CaO2的装置示意图如下:
CaO2(s),在纯氧条件下,制取CaO2的装置示意图如下:
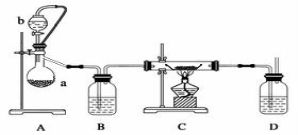
请回答下列问题:
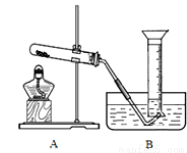
(1)装置A中反应的化学方程式为 ;装置D中盛有的液体是浓硫酸,其作用一是观察氧气的流速,判断氧气通入是否过快及氧气与钙反应进行的程度;二是 。
仪器安装后应进行的实验操作:A通入氧气 B检查装置气密性 C加入药品 D停止通氧气 e.点燃酒精灯 f.熄灭酒精灯 g.冷却至室温,正确的操作顺序为 。
(2)利用反应Ca2++H2O2+2NH3·H2O+6H2O=CaO2·8H2O+2NH4+,在碱性环境中,制取CaO2的流程示意图如下:
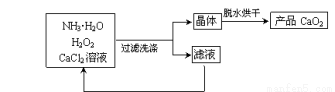
请回答下列问题:
①反应中,NH3·H2O在Ca2+和H2O2的反应历程中所起的作用是_____________ _;洗涤CaO2·8H2O晶体时,判断晶体是否完全洗净的试剂为 ;滤液循环使用时需在反应器中加入一种物质,该物质的化学式为 。
②利用反应2CaO2==2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置示意图如右:若直接读数确定25℃、1大气压下气体的体积,则测量结果__________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com