
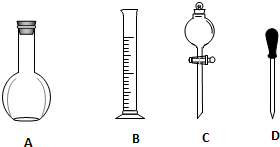
分析 (1)配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶,依据操作步骤选择需要的仪器;
(2)容量瓶是一种精密仪器,容积会随着温度的改变而改变,故不能受热,不能用来存储溶液,溶解固体,稀释浓溶液,在使用前应查漏,据此分析;
(3)依据m=CVM计算需要溶质的质量;定容时仰视刻度线,导致溶液体积偏大,依据C=$\frac{n}{V}$进行误差分析;
(4)依据c=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度,依据溶液稀释前后溶质的物质的量不变计算需要浓硫酸的体积,依此选择合适的量筒.
解答 解:(1)配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶,用到的仪器:托盘天平、药匙、量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管,用不到的仪器:平底烧瓶、分液漏斗,还缺少的仪器:烧杯、玻璃棒、500mL容量瓶;
故答案为:A、C 烧杯、玻璃棒、500mL容量瓶;
(2)A、配制溶液时要摇匀,应检验容量瓶是否漏液,故A正确;
B.容量瓶用水洗净后,不能用待配溶液洗涤,否则会引起溶质的物质的量偏多,则所配溶液浓度偏大,故B错误;
C.容量瓶不能用来溶解固体,故C错误;
D.容量瓶不能用来稀释浓溶液,故D错误;
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀,故E正确;
故选:BCD;
(3)需要0.1mol/LNaOH溶液450mL,应选择500mL容量瓶,需要溶质的质量m=0.1mol/L×0.5L×40g/mol=2.0g;定容时仰视刻度线,导致溶液体积偏大,依据C=$\frac{n}{V}$可知溶液浓度偏低;
故答案为:2.0 小于;
(4)质量分数为98%、密度为1.84g/cm3的浓硫酸的物质的量浓度=$\frac{1000×1.84g/ml×98%}{98g/mol}$=18.4mol/L,浓硫酸稀释前后溶质的物质的量不变,设浓硫酸的体积为V,所以18.4mol/L×V=0.5/L×0.5L,V=0.0136L=13.6mL,应选择15ml量筒;
故答案为:13.6;15.
点评 本题考查一定物质的量浓度溶液的配制,熟悉配制原理、注意容量瓶、量筒规格的选取方法,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.3 mol•L-1的Na2SO4溶液中含有的Na+和SO42-的总物质的量为0.9 mol | |
| B. | 当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol•L-1,只有当22.4 L氨气溶于水制得1 L氨水时,其浓度才是1 mol•L-1 | |
| C. | 在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同 | |
| D. | 10℃时,0.35 mol•L-1的KCl饱和溶液100 mL蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.8 | 2.4 | 0.4 | 放出热量:Q |
| A. | 容器①、②中反应的平衡常数相等,平衡时氮气的转化率相等 | |
| B. | 平衡时,两个容器中NH3 的体积分数均为1/8 | |
| C. | 容器②中达平衡时放出的热量Q=4.63 kJ | |
| D. | 若容器①改为恒压体系,充入0.25 L He,则平衡时放出的热量大于23.15 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
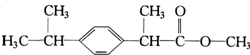 某种药物主要成分X的分子结构如图,关于有机物X的说法中错误的是( )
某种药物主要成分X的分子结构如图,关于有机物X的说法中错误的是( )| A. | ①④ | B. | ②④ | C. | ②③ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
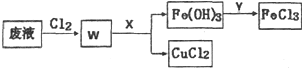 铜及其化合物在工农业生产中有着广泛的用途.
铜及其化合物在工农业生产中有着广泛的用途.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
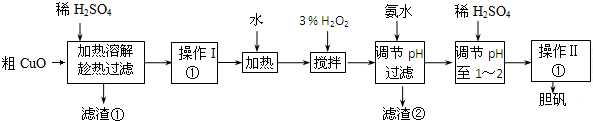
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠的电离方程式为:NaHCO3═Na++HCO3- HCO3-?H++CO32- | |
| B. | 偏铝酸钠的水解方程式为:AlO2-+2H2O═Al(OH)3↓+OH- | |
| C. | 硫化铝溶于水的水解方程式为:Al2S3+6H2O═2Al(OH)3↓+3H2S↑ | |
| D. | 醋酸铵的水解方程式为:CH3COO-+NH4++H2O?CH3COOH+NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com