
铬酸铅俗称铬黄,不溶于水。广泛用于涂料、油墨、漆布、塑料和文教用品等工业。实验室模拟工业上用铬污泥(含有Cr2O3、Fe2O3、A12O3、SiO2等)制备铬黄的工艺流程如下: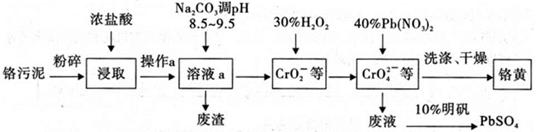
(1)将铬污泥粉碎的目的是 ,操作a的名称为 ;
(2)废渣的主要成分是A1(OH)3和Fe(OH)3。已知25℃时,A1(OH)3的Ksp=1.3×10-33,则该温度下反应Al3++3H2O Al(OH)3+3H+的平衡常数为 (保留两位有效数字);
Al(OH)3+3H+的平衡常数为 (保留两位有效数字);
(3)写出加入30%H2O2过程中发生的离子反应方程式: ;
(4)实验室洗涤铬黄沉淀的方法: ;
(5)写出浓盐酸与A12O3反应的离子方程式: 。
(14分)(1)增大接触面积,提高浸取率(2分) 过滤(2分)
(2)7.7×10-10(2分)
(3)2CrO2-+3H2O2+2OH-=2CrO42-+4H2O(3分)
(4)加蒸馏水浸没铬黄沉淀,等蒸馏水流尽后,再重复操作1~2次(3分)
(5)Al2O3+6H+=2Al3++3H2O(2分)
解析试题分析:(1)铬污泥含有固体反应物,固体粉碎的目的是增大固体反应物的表面积,增大化学反应速率,提高铬等元素的浸取率;氧化铬、氧化铁是碱性氧化物,易溶于过量的浓盐酸,得到含有CrCl3、FeCl3的溶液,氧化铝是两性氧化物,溶于过量的浓盐酸,得到含有AlCl3的溶液,二氧化硅是酸性氧化物,不溶于盐酸,则操作a为过滤,目的是除去SiO2;(2)溶液a中加入适量Na2CO3调pH8.5~9.5时,碳酸根离子与氢离子容易反应生成二氧化碳和水,碳酸根离子与铁离子容易发生双水解反应,生成氢氧化铁沉淀和二氧化碳,碳酸根离子与铝离子容易发生双水解反应,生成氢氧化铝沉淀和二氧化碳,再次过滤所得废渣的主要成分是A1(OH)3和Fe(OH)3,碳酸根离子水解促进铬离子水解,但是铬离子的水解没有进行到底,导致滤液中主要成分是NaCrO2、NaCl等的溶液;由于25℃时H2O H++OH-,则Kw=1.0×10-14;由于Al(OH)3(s)
H++OH-,则Kw=1.0×10-14;由于Al(OH)3(s)  Al3++3OH-,则Ksp[Al(OH)3]=c(Al3+)?c3(OH-)=1.3×10-33;由于Al3++3H2O
Al3++3OH-,则Ksp[Al(OH)3]=c(Al3+)?c3(OH-)=1.3×10-33;由于Al3++3H2O Al(OH)3+3H+,则K=
Al(OH)3+3H+,则K= =
= =
= =
= ≈7.7×10-10;
≈7.7×10-10;
(3)pH=8.5~9.5时,溶液呈碱性,CrO2-变为CrO42-是氧化反应,铬元素的化合价由+3价升为+6价,由此推断H2O2是该反应的氧化剂,氧元素由—1价降为—2价,则还原产物是水,根据电子、电荷、原子个数守恒原理配平,该过程的离子方程式为2CrO2-+3H2O2+2OH-=2CrO42-+4H2O;(4)洗涤沉淀时,一般是向沉淀中加蒸馏水至浸没铬黄沉淀,等蒸馏水流尽后,再重复操作1~2次;(5)氧化铝是两性氧化物,盐酸是强酸溶液,二者反应生成氯化铝和水,氯化铝是易溶易电离的盐,则该反应为Al2O3+6H+=2Al3++3H2O。
考点:考查物质制备工艺流程,涉及铬污泥粉碎的目的、水的离子积和氢氧化铝溶度积的计算表达式、铝离子水解平衡常数的计算、氧化还原反应、离子方程式、洗涤铬黄沉淀的方法、氧化铝与浓盐酸反应的离子方程式等。


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:填空题
废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法可回收WC和Co,工艺流程简图如下: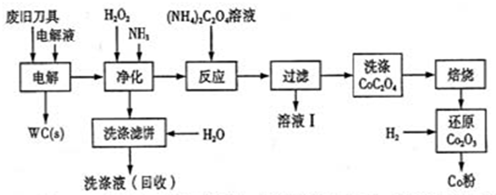
(1)电解时废旧刀具做阳极,不锈钢做阴极,HCl溶液为电解液,阴极主要的电极反应为 ;
(2)净化步骤所得滤饼的主要成分是Fe(OH)3,回收的洗涤液代替水配制电解液,目的是回收利用其中的 ;
(3)溶液I的主要成分是NH4Cl,洗涤CoC2O4不充分对最终产品纯度并无明显影响,但焙烧时会造成环境污染,原因是 ;
(4)将Co2O3还原成Co粉的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀
有气体进行稀释,同时需要避免光照、震动或加热。实验室以电解法制备ClO2的流程如下:
(1)ClO2中所有原子_____________(填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用_________
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.蒸馏水
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是( )
A.二氧化氯可广泛用于工业和饮用水处理
B.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
C.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备。化学反应方程式为_____________________________。缺点主要是产率低、产品难以分离,还可能污染环境。
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是 ___________________,此法相比欧洲方法的优点是____________________________。
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸
钠,化学反应方程式为______________________________________________________。
此法提高了生产及储存、运输的安全性,原因是 _________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业利用精炼镁渣(含有MgO、KCl、MgCl2、BaCl2、CaCl2、FeCl3等杂质)回收MgCl2的工业流程如下:
已知:25℃时有关物质的溶度积如下:
| 物质 | CaCO3 | MgCO3 | BaCO3 | Mg(OH)2 | Fe (OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 5.1×10-9 | 5.61×10-12 | 2.64×10-38 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如下图所示: 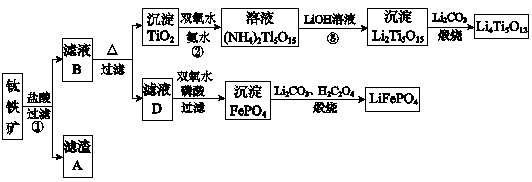
已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O
(1)化合物FeTiO3中铁元素的化合价是 。
(2)滤渣A的成分是 。
(3)滤液B中TiOCl42- 转化生成TiO2的离子方程式是 。
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如下图所示。反应温度过高时,Ti元素浸出率下降的原因是 。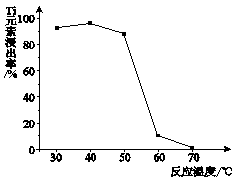
(5)反应③的化学方程式是 。
(6)由滤液D制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是 。
(7)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)作电极组成电池,其工作原理为:Li4Ti5O12+3LiFePO4 Li7Ti5O12+3FePO4
Li7Ti5O12+3FePO4
该电池充电时阳极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式。SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备的工艺流程如下: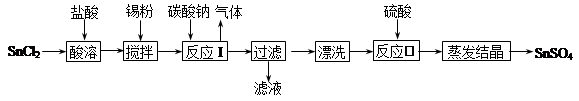
回答下列问题:
(1) SnCl2用盐酸而不用水直接溶解的原因是 ,加入锡粉的作用是 。
(2) 反应I生成的沉淀为SnO,写出该反应的化学方程式:
。
(3) 检验沉淀已经“洗涤”干净的操作是: 。
(4)反应II硫酸的作用之一是控制溶液的pH。若溶液中c(Sn2+)=1.0mol·L-1,则室温下应控制溶液pH 。(已知:Ksp[Sn(OH)2]=1.0×10-26)
(5)酸性条件下,SnSO4还可用作双氧水的去除剂,试写出所发生反应的离子方程式:
。
(6)潮湿环境中,镀锡铜即使锡层破损也能防止形成铜绿,请结合有关的原理解释其原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在硫酸的工业制法中,下列生产操作与说明生产操作的主要原因二者都正确的是( )
| A.硫铁矿煅烧前将要矿粒粉碎,因为大块的硫铁矿不能燃烧 |
| B.从沸腾炉出来的炉气需净化,因为炉气中SO2会与杂质反应 |
| C.SO2氧化为SO3时需使用催化剂,这样可以提高SO2的转化率 |
| D.SO3用质量分数为98%的浓H2SO4吸收,目的是防止形成酸雾,以便使SO3吸收完全 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某地农田土壤胶体的胶粒带负电荷,若在该农田里施用含氮量相等的下列化肥,有效成分利用率最差的是 ( )。
| A.(NH4)2SO4 | B.NH4HCO3 |
| C.NH4NO3 | D.NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关工业生产的叙述正确的是( )
| A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 |
| C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
| D.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com