
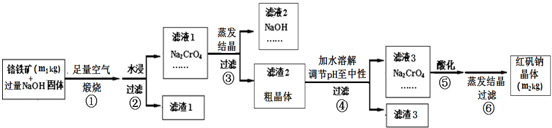
 �Ѱۣ���Ҫ�ɷ���Ti02������������ǿ�������ʸߣ������㷺�������ᡢ���ϡ���ֽ����ҵ�����������Ҵ���ˮ������Ĵ�������ͼ������������Ҫ�ɷ�FeTi03������������Ϊ��Ҫԭ�������Ѱ۵Ĺ�������ͼ���ش��������⣺
�Ѱۣ���Ҫ�ɷ���Ti02������������ǿ�������ʸߣ������㷺�������ᡢ���ϡ���ֽ����ҵ�����������Ҵ���ˮ������Ĵ�������ͼ������������Ҫ�ɷ�FeTi03������������Ϊ��Ҫԭ�������Ѱ۵Ĺ�������ͼ���ش��������⣺| 0.015 |
| 0.01 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||
B��
| ||
| C��M?NA g | ||
D��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����������Ҫ�ɷ���Fe3O4 |
| B������ʯ����Ҫ�ɷ����������Ҫ�ɷ���ͬ |
| C���������ĩ�����������KSCN��Һ����Һ���ɫ |
| D��FeO�׳����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A | B | C | D | |
| �о�Ŀ�� | ѹǿ�Է�Ӧ��Ӱ�� | �¶ȶԷ�Ӧ��Ӱ�� | ����O2Ũ�ȶԷ�Ӧ��Ӱ�� | Ũ�ȶ�ƽ�ⳣ����Ӱ�� |
| ͼʾ |  |  |  |  |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| �ᾧ�¶�/�� | Na2CrO4�־��и����ʺ���/w% | |||
| Na2CrO4?4H2O | NaOH | Na[Al��OH��4] | Na2SiO3 | |
| 30 | 52.45 | 29.79 | 8.69 | 12.21 |
| 40 | 68.81 | 20.49 | 8.46 | 10.84 |
| 50 | 60.26 | 27.96 | 10.36 | 9.32 |
| 60 | 50.74 | 29.66 | 10.40 | 12.25 |
| 70 | 46.77 | 33.06 | 8.10 | 6.48 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����pH��ֽ���ij������ˮ��pHֵΪ3.5 |
| B����ⷨ����ͭ������ͭ�ӵ�Դ������ |
| C�����Ȼ���������������ˮ�У������Ȼ�����Һ |
| D�����Ȼ�����Һ�������ɣ������գ��͵õ��Ȼ������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com