
【题目】二氧化碳的捕捉、封存与再利用是实现温室气体减排的重要途径之一。
(1)二氧化碳的电子式为___________。
(2)下列利用二氧化碳的反应中原子利用率达100%的是_________(填序号)。
a.CO2+2NH3 ![]() CO(NH2)2+H2O
CO(NH2)2+H2O
b.CO2+CH4![]() CH3COOH
CH3COOH
c.CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
d.![]()
(3)一种正在开发的利用二氧化碳制取甲醇的流程如下:
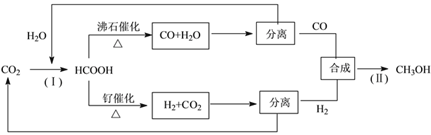
①反应(Ⅰ)将CO2和H2O转化为甲酸常用途径有两种,如下图(a)和(b)。
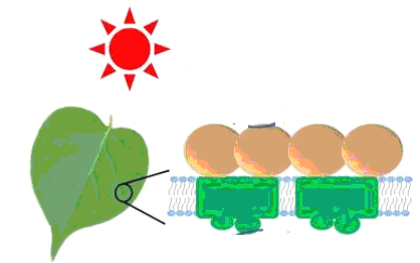
图(a)中能量主要转化方式为___________,图(b)中发生反应的化学方程式为___________。
②在5L的恒温恒容密闭容器中充入1moLCO和4molH2,加入催化剂发生反应,测得CO及CH3OH的物质的量随时间变化如下图所示。
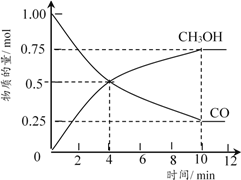
图中第___________min(填数字)反应达到平衡,CO在0~4min内的平均反应速率比在4~8min内的快,其原因是___________;达到平衡时氢气的浓度为___________。
【答案】 ![]() bd 光能转变为化学能 2CO2+2H2O
bd 光能转变为化学能 2CO2+2H2O![]() 2HCOOH + O2 10 随着反应的进行CO的浓度不断变小(或容器内气体的压强不断减小) 0.5mol·L-1
2HCOOH + O2 10 随着反应的进行CO的浓度不断变小(或容器内气体的压强不断减小) 0.5mol·L-1
【解析】(1)二氧化碳的电子式为![]() ;(2)b、d为加成反应和加聚反应,产物只有一种,二氧化碳在反应中原子利用率达100%,答案选bd;(3)①图(a)中能量主要转化方式为光能转变为化学能;根据图中信息可知,图(b)中发生反应为二氧化碳与水在通电作用下转化为甲醛和氧气,其化学方程式为:2CO2+2H2O
;(2)b、d为加成反应和加聚反应,产物只有一种,二氧化碳在反应中原子利用率达100%,答案选bd;(3)①图(a)中能量主要转化方式为光能转变为化学能;根据图中信息可知,图(b)中发生反应为二氧化碳与水在通电作用下转化为甲醛和氧气,其化学方程式为:2CO2+2H2O![]() 2HCOOH + O2;②根据图中信息可知,在第10min时各物质的量不再改变,反应达到平衡;随着反应的进行CO的浓度不断变小(或容器内气体的压强不断减小),CO在0~4min内的平均反应速率比在4~8min内的快;根据反应CO+2H2=CH3OH,达到平衡时CO由1mol降到0.25mol,则氢气由4mol应降到2.5mol,氢气的浓度为:
2HCOOH + O2;②根据图中信息可知,在第10min时各物质的量不再改变,反应达到平衡;随着反应的进行CO的浓度不断变小(或容器内气体的压强不断减小),CO在0~4min内的平均反应速率比在4~8min内的快;根据反应CO+2H2=CH3OH,达到平衡时CO由1mol降到0.25mol,则氢气由4mol应降到2.5mol,氢气的浓度为:![]() =0.5mol·L-1。
=0.5mol·L-1。


科目:高中化学 来源: 题型:
【题目】实验室以软锰矿(主要成分为MnO2,还有少量FeO、Fe2O3、MgO和Al2O3杂质)为原料制备高锰酸钾的流程如下图:

(1) “酸浸”需要加热的目的是__________,此过程中发生反应的离子方程式是______________。(任写一条)
(2) “熔融”过程中,MnO2被KC1O3氧化成K2MnO4。
①该反应的化学方程式为_____________________。
②加入KC1O3应过量的原因除了提高MnO2利用率,还有_________________.
③将适量KClO3和KOH混合均匀后在坩埚内高温反应,应选用坩埚为__________。(选填序号)
a.石英坩埚 b.铁坩埚 c.氧化铝坩埚
(3)己知:①MnO42-只存在于强碱环境(pH>13.5)中,当pH降低时,MnO42-会歧化为MnO4-和MnO2;②饱和碳酸钾溶液的pH约为12.3,饱和碳酸氢钾溶液的pH约为8.8;③相关物质的溶解度曲线如下图。

请补充完整由浸取液制备KMnO4晶体的实验方案:向浸取液中缓缓通入CO2,_____________,低温供干得KMnO4晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 标准状况下,2.24 L苯中含有碳碳双键数为0.3NA
B. 14g由乙烯和丙烯组成的混合气体中含氢原子数为2NA
C. 0.1molCH4与0.1molCl2混合充分光照,生成CH3Cl分子数为0.1 NA
D. 0.1molN2和0.3molH2在高温、高压及催化剂下充分反应,产物的分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硼镁泥(主要成分为MgSiO3、Fe2O3及少量Al2O3、FeO和MnO)为原料制备高纯Mg(OH)2的流程如下:
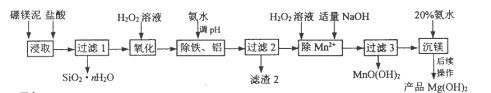
己知:
①常温下此体系中各氢氧化物开始沉淀与沉淀完全时的pH范围如下表所示:
pH值 | Mg(OH)2 | Mn(OH)2 | MnO(OH)2 | Fe(OH)2 | Al(OH)3 | Fe(OH)3 |
开始沉淀时 | 9.3 | 7.1 | 7.8 | 7.6 | 3.7 | 2.3 |
沉淀完全时 | 10.8 | 10.8 | 9.8 | 9.6 | 4.7 | 3.7 |
②温度高于340℃时Mg(OH)2开始分解为MgO和H2O。
(1)“浸取”时,为提高镁的浸取率可行的措施为__________。
a.将硼镁泥制成浆料 b.降低浸取温度 c.用盐酸多次浸取
(2)“浸取”时,MgSiO3与盐酸反应的化学方程式为_________________________。
(3)“除铁、铝”时,需调节溶液pH范围为_________________________。
(4)“除Mn2+”时发生反应的离子方程式为_________________________;
过滤3所得滤渣中含有MnO(OH)2和__________。
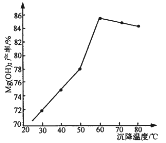
(5)“沉镁”时,反应温度与Mg(OH)2的产率如图所示,当温度超过60℃,随温度再升高,Mg(OH)2产率反而降低,其原因可能是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列说法正确的是( )
A.1mol OH﹣中含有9NA个电子
B.28g的CO气体中含有NA个氧原子
C.1L 1mol/L的AlCl3溶液中含有NA个Al3+
D.常温常压下11.2 L的甲烷气体含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列溶液中水的电离程度最小的是( )
A.0.01 mol/L盐酸
B.0.01 mol/L Na2CO3溶液
C.pH=4 NaHSO3溶液
D.pH=11氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向沸水中滴加几滴饱和氯化铁溶液并继续煮沸至溶液呈红褐色时停止加热,此时当光束通过该红褐色液体时,从侧面可观察到一条光亮的“通路”说明该红褐色液体是
A.溶液 B.胶体 C.悬浊液 D.乳浊液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com