
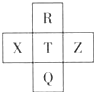
 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A、非金属性:Z<T<X |
| B、R与Q原子核外电子数相差26 |
| C、气态氢化物稳定性:R<T<Q |
| D、最高价氧化物的水化物的酸性:X>T |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
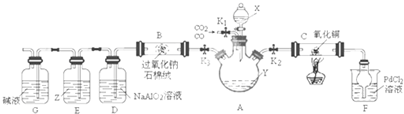
| 组别 | 实验操作 | 实验现象或数据 | 结 论 | ||
| 甲 | ①向a g M中加入一定量稀硫酸,充分搅拌; ②继续滴加稀硫酸至过量,充分反应. |
①固体明显减少; ②仍然有一定量固体,溶液呈蓝色 |
①M中一定有Cu2O; ②M中一定有Cu. | ||
| 乙 | ①将甲实验后所得溶液过滤 ②将滤渣洗涤、干燥、称量 |
滤渣质量为
|
M为Cu和Cu2O的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氮气的电子式:N??N |
| B、乙烯的结构简式:CH2CH2 |
| C、二氧化碳分子的结构式:O-C-O |
D、CH4分子的球棍模型: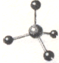 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同 |
| B、制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 |
| C、用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 |
| D、用AgNO3溶液可以鉴别KCl和KI |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、1:3 |
| C、1:6 | D、3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属原子的核外电子在金属晶体中都是自由电子 |
| B、镁型和铜型的原子堆积方式空间利用率最高 |
| C、金属原子在化学变化中失去的电子数越多,其还原性越强 |
| D、金属导电的实质是金属阳离子在外电场作用下的定向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中导电粒子的数目减少 |
| B、再加入10mLpH=11的NaOH溶液,混合液的pH=7 |
| C、溶液中c(OH-)增大 |
| D、醋酸的电离程度增大,c(H+)亦增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L |
| B、2mol/L |
| C、3 mol/L |
| D、4 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com