
对于反应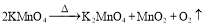 ,下列说法错误的是
,下列说法错误的是
A.氧化剂和还原剂都是KMnO4
B.该反应的还原产物只有MnO2
C.该反应的氧化产物是O2
D.KMnO4中Mn元素表现氧化性,O元素表现还原性
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:推断题
(9分)有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙 、H ;
(2)写出反应②的离子方程式: ;
(3)写出金属A与水反应的离子方程式 ;
(4)F与D溶液反应后的产物在空气中转化为H的化学方程式 ;现象为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:选择题
下列关于晶体结构和性质的叙述中,错误的是
A.分子晶体中一定存在共价键
B.原子晶体中一定存在共价键
C.金属晶体通常具有导电、导热和良好的延展性
D.离子晶体在固态时不导电,在熔化状态下能导电
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:填空题
已知:CH4(g)+2O2(g)→CO2(g)+2H2O(l)+Q1;2H2+O2(g)→2H2O(g)+Q2;2H2+O2(g)→2H2O(l)+Q3;
若体积比为4:1的甲烷与氢气的混合气体11.2L(S.T.P)在氧气中完全燃烧,恢复至室温,放出的热量为_________________(表达式)。
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
对于铜锌原电池实验后得出的结论和认识中,正确的是
A.构成原电池正极和负极的材料必须是两种金属
B.由铜、锌电极与硫酸铜溶液组成的原电池中铜是负极
C.电子由锌片流经稀硫酸溶液到铜片,氢离子在铜片上得到电子放出氢气
D.铜锌原电池工作时,若有13g锌被溶解,电路中就有0.4mol电子通过
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.有单质生成的分解反应一定是氧化还原反应
B.某元素从化合态变为游离态时,该元素一定被还原
C.氧化剂被氧化,还原剂被还原
D.没有氧元素参加的反应一定不是氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
分类是科学研究的重要方法,下列物质分类不正确的是
A.化合物:干冰,冰水混合物,烧碱,小苏打
B.非电解质:乙醇,四氯化碳,氯气,葡萄糖
C.同素异形体:活性炭,C60,C80,金刚石
D.混合物:漂白粉,纯净矿泉水,分析纯盐酸,石灰石
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三一模理综化学试卷(解析版) 题型:选择题
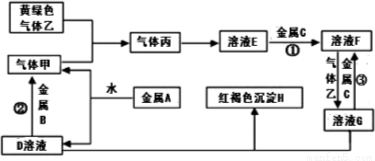
下列说法正确的是
A.①表示化学反应2NO2(g) + O3(g)  N2O5(g) + O2(g)△H> 0
N2O5(g) + O2(g)△H> 0
B.②表示25℃时,用0.1 mol/LCH3COOH溶液滴定20 mL 0.1 mol/LNaOH溶液,溶液的pH随加入酸体积的变化
C.③表示10 mL 0.01 mol/L KMnO4酸性溶液与过量的0.1 mol/LH2C2O4溶液混合时,n (Mn2+)随时间的变化
D.④表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广西玉林市博白县高三下学期返校调研考试化学试卷(解析版) 题型:实验题
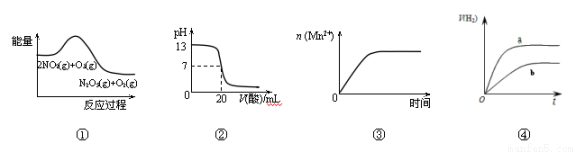
(14分)半导体生产中常需要控制掺杂,以保证控制电阻率。三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)
已知黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5 PCl3遇水会强烈水解生成 H3PO3和HC1。遇O2会生成POCl3,POCl3溶于PCl3,PCl3、POCl3的熔沸点见下表:
物质 | 熔点/℃ | 沸点/℃ |
PCl3 | -112 | 75.5 |
POCl3 | 2 | 105.3 |
请回答下列问题:
(1)A装置中制氯气的离子方程式为 。
(2)B中所装试剂是 ,
E中冷水的作用是 ,
F中碱石灰的作用是____ 。_
(3)实验时,检査装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷。通干燥CO2的作用是 。
(4)粗产品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后.通过_____(填实验操作名称),即可得到较纯净的PCl3。
(5)通过下面方法可测定产品中PCl3的质量分数
①迅速称取1.00 g产品,加水反应后配成250 mL溶液;
②取以上溶液25.00 mL,向其中加入10.00 mL 0.1000 mol·L-1碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000 mol·L-1的Na2S2O3,溶液滴定②重复②、③操作,平均消耗Na2S2O3,溶液8.40 mL
已知:H3PO3+H2O+I2 =H3PO4+2HI,I2+2Na2S2O3 = 2NaI+Na2S4O6,假设测定过程中没有其他反应。根据上述数据,该产品中PC13的质量分数为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com