
【题目】有机化合物K是一种聚酯材料,合成路线如下:

己知:①AlCl3为生成A的有机反应的催化剂
②F不能与银氨溶液发生反应,但能与Na反应。
(1)生成A的有机反应类型为________。生成A的有机反应分为以下三步:
第一步:CH3COCl+AlCl3→CH3CO++AlCl4,
第二步:____________________
第三步:AlCl4-+H+→AlCl3+HCl
请写出第二步反应。
(2)B的化学名称为反应条件①为______________,反应条件②为_______________。
(3)由乙炔生成F的化学方程式为____________________。
(4)F的同分异构体很多,其中能同时满足这以下4个条件的链状化合物共有_________种(包括顺反异构和对映异构);
①含有三种官能团;②能与新制的Cu(OH)2悬浊液反应;③氧原子不与碳碳双键相连
④与Na反应可放出氢气
(5)K的结构简式为_________________。
(6)请以乙炔和丙酮为原料,按照加成、加成、消去的反应类型顺序三步合成天然橡胶的单体。(无机试剂任选)________________
【答案】 取代反应 C6H6+CH3CO+→C6H5COCH3+ H+ 1-苯基乙醇(或1-苯基-1-乙醇) 浓硫酸、加热 氢氧化钠水溶液、加热 5 ![]()
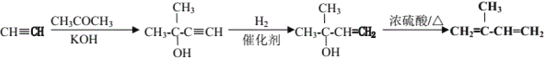
【解析】试题分析:由合成路线及题中信息可知,苯与氯乙酰发生取代反应生成A,A为苯乙酮;A与氢气发生加成反应生成1-苯基乙醇,C到D的反应条件为加成反应的条件,则B到C发生了消去反应,C为苯乙烯,该反应的条件为浓硫酸作催化剂、加热,D为1,2-二溴苯乙烷;因为K为聚酯,所以,D到E为卤代烃的水解反应,则E为1-苯基-1,2-乙二醇;乙炔与甲醛发生加成反应生成F,F不能与银氨溶液发生反应,但能与Na反应,故F为丁炔二醇;F与氢气发生加成反应生成G,G为1,4-丁二醇,G再发生催化氧化生成H,H为1,4-丁二醛,H经银氨溶液氧化、酸化得到I,I为1,4-丁二酸。所以K为聚1,4-丁二酸苯乙二酯(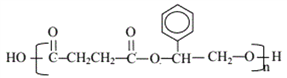 )。
)。
(1)生成A的有机反应类型为取代反应。生成A的有机反应分为以下三步,由总反应和第一步、第三步反应,可以写出第二步反应为:C6H6+CH3CO+→C6H5COCH3+ H+。
(2)B的化学名称为1-苯基乙醇(或1-苯基-1-乙醇),反应条件①为浓硫酸、加热,反应条件②为氢氧化钠水溶液、加热。
(3)由乙炔生成F的化学方程式为![]() 。
。
(4)F(![]() )的同分异构体很多,其中能同时满足以下4个条件:①含有三种官能团;②能与新制的Cu(OH)2悬浊液反应,说明其分子中有醛基;③氧原子不与碳碳双键相连;④与Na反应可放出氢气,则其分子中有羟基。这样的链状化合物有HOCH2CH=CHCHO(有顺反异构)、CH2=C(CH2OH)CHO、CH2=CHCHOHCHO(有对映异构体),所以共有5种(包括顺反异构和对映异构);
)的同分异构体很多,其中能同时满足以下4个条件:①含有三种官能团;②能与新制的Cu(OH)2悬浊液反应,说明其分子中有醛基;③氧原子不与碳碳双键相连;④与Na反应可放出氢气,则其分子中有羟基。这样的链状化合物有HOCH2CH=CHCHO(有顺反异构)、CH2=C(CH2OH)CHO、CH2=CHCHOHCHO(有对映异构体),所以共有5种(包括顺反异构和对映异构);
(5)K的结构简式为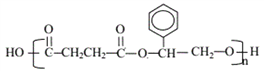 。
。
(6)乙炔和丙酮为原料,按照加成、加成、消去的反应类型顺序三步合成天然橡胶的单体异戊二烯,根据题中信息,首先乙炔和丙酮发生加成反应,然后加成产物与氢气再发生加成反应,最后与浓硫酸加热发生消去反应,具体合成路线如下: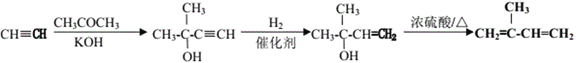 。
。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如图所示的装置进行原电池原理的探究。下列叙述错误的是

A. a和b不连接时,锌片上有气体生成,该装置不能形成原电池
B. a和b用导线连接时铜片为正极,发生的反应式为:2H++2e-=H2↑
C. a和b用导线连接时,电子由Zn经导线流向Cu,再经稀硫酸流回Zn
D. 无论a和b是否连接,稀硫酸均参与反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对利用甲烷消除NO2污染进行研究,CH4+2NO2![]() N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
组别 | 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | 0.15 |
下列说法正确的是( )
A. 由实验数据可知实验控制的温度T2>T1
B. 组别①中,0~20min内,NO2的降解速率为0.0125mol·L-1·min-1
C. 40min时,表格中T2对应的数据为0.18
D. 0~10min内,CH4的降解速率①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的说法错误的是( )
A.原电池是将化学能转化为电能的装置
B.原电池负极发生氧化反应
C.原电池中,阳离子向负极移动
D.原电池电子流出的一极为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,向100 mL含氯化氢14.6 g的盐酸溶液里放入5.60 g纯铁粉(不考虑反应前后溶液体积的变化),反应开始至2 min末,收集到1.12 L(标准状况)氢气。在此之后,又经过4 min,铁粉完全溶解。则:
(1)在前2 min内用FeCl2表示的平均反应速率是。
(2)在后4 min内用HCl表示的平均反应速率是。
(3)前2 min与后4 min相比,反应速率较快的是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,按熔点由低到高的顺序排列正确的是( )
①O2、I2、Hg ②PH3、AsH3、NH3 ③Na、K、Rb④Na、Mg、Al
A. ①③ B. ①④
C. ②③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌元素对婴儿及青少年的智力和身体发育有重要的作用,被称为生命火花。利用恒电势电解NaBr溶液间接将葡萄糖[CH2OH(CHOH)4CHO]氧化为葡萄糖酸[CH2OH(CHOH)4COOH],进而制取葡萄糖酸锌,装置如图所示,下列说法错误的是

A. 钛网与直流电源的正极相连
B. 石墨电极的反应为:2H2O+2e-=H2↑+2OH-
C. 电解过程中硫酸钠溶液浓度保持不变
D. .生成葡萄糖酸的方程式为:CH2OH(CHOH)4CHO+Br2+H2O=CH2OH(CHOH)4COOH+2HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2NO2![]() 2N0+O2在密闭容器中反应,达到平衡状态的标志是( )
2N0+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成nmolO2的同时生成2nmolNO2
②单位时间内生成nmolO2的同时生成2nmolNO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : l 的状态
④混合气体的颜色不再改变的状态
A. ①④ B. ②③ C. ①③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2mol A和2molB 两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,请填写下列空白:
xC(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,请填写下列空白:
(1)x值等于;
(2)A的转化率为;
(3)如果增大反应体系的压强,则平衡体系中C的质量分数(增大、减小、不变)
(4)如果上述反应在相同条件下从逆反应开始进行,开始加入C和D各4 /3mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入B物质 mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com