
【题目】在恒容密闭容器中发生反应:2NO2(g)![]() N2O4(g) ΔH=-a kJ/mol(a>0),设NA为阿伏加德罗常数的值。下列说法错误的是( )
N2O4(g) ΔH=-a kJ/mol(a>0),设NA为阿伏加德罗常数的值。下列说法错误的是( )
A.平衡后升高温度,容器中气体颜色加深
B.每消耗44.8 LNO2,生成N2O4的分子数一定为NA
C.该容器中气体质量为46 g时,原子总数为3NA
D.若N2O4分子数增加0.5NA,则放出0.5a kJ的热量
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.熔融状态下硫酸氢钾中的离子键、共价键均被破坏,形成定向移动的离子,因而能够导电
B.F2、Cl2、Br2、I2的熔沸点逐渐升高,是因为分子间作用力越来越大
C.NH3和Cl2两种分子中,每个原子的最外层都达到8电子的稳定结构
D.HF、HCl、HBr、HI的稳定性逐渐减弱,沸点逐渐升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水四氯化锡(SnC14)是一种用途广泛的化工中间体,常用作媒染剂和有机合成的氯化催化剂。熔融的金属锡(熔点231℃)在300℃左右能直接与Cl2作用生成无水四氯化锡,实验室装置如图所示:

已知信息如下:①将金属锡熔融,通人干燥氯气进行反应,生成四氯化锡。②无水四氯化锡是无色易流动的液体,熔点为一33℃,沸点为114.1℃。二氯化锡是无色晶体,熔点为246℃,沸点为652℃。③无水四氯化锡在空气中极易水解,水解产物之一是SnO2.xH2O,并产生白烟。请回答下列问题:
(l)开始实验前一定要____,E中冷水的作用是 ___。
(2)装置F中盛放的最佳试剂为 ___,作用是____。
(3)实验时应先打开A处分液漏斗旋塞和整套装置的阀门,待观察到____这一现象时,再点燃D处酒精灯。
(4)若撤去装置C,则D中还可能发生反应的化学方程式为 __。
(5) Cl2和锡作用即可生成SnC14,也会生成SnCl2,为减少SnCl2的生成,可采取的措施是 _______ .
(6)得到的产物中常含有杂质SnCl2,SnCl2是常用的还原剂。某实验小组用碘氧化法滴定分析产品中杂质SnCl2的质量分数。准确称取a克该样品于锥形瓶,用适量浓盐酸溶解,淀粉溶液作指示剂,c mol.L-l碘标准溶液滴定至终点,消耗标准液20. 00mL,已知滴定原理是:SnCl2+2HCl+I2=SnC14+2HI,则产品中杂质SnCl2的质量分数为____(用含a、c的代数式表示);即使此法测定的操作均正确,但测得的SnCl2含量仍低于实际含量,其原因可能是________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“点击化学”是指快速、高效连接分子的一类反应,例如铜催化的Huisgen环加成反应:

我国科研人员利用该反应设计、合成了具有特殊结构的聚合物F并研究其水解反应。合成线路如下图所示:
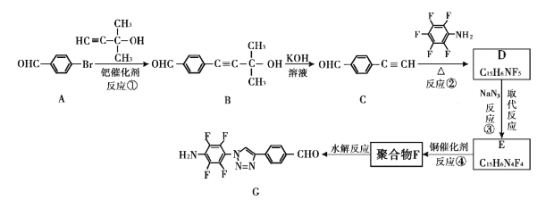
已知:![]()
(1)A生成B的反应类型是____。
(2)关于B和C,下列说法正确的是____(填字母序号)。
a 利用核磁共振氢谱可以鉴别B和C b B不能发生消去反应 c 可用酸性高锰酸钾溶液检验C中含醛基
(3)B生成C的过程中还有另一种生成物X,分子式为C3H6O,核磁共振氢谱显示只有一组峰,X的结构简式为 ___。
(4)反应②的化学方程式为 ___。
(5)请根据以上流程,并推测聚合物F所具有的特殊结构,下列关于聚合物F的结构说法正确的是___
A F中必含 -CH2=N- 结构
B F中必含 -N=N- 结构
C F的结构可能是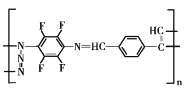
(6)H是比A多一个碳原子的同系物。H的同分异构体中符合下列条件的有 ___种。
①苯环上有三个取代基 ②能和FeCl3发生显色反应
(7)为了探究连接基团对聚合反应的影响,设计了单体K,其合成路线如下,写出H、I、J的结构简式:___
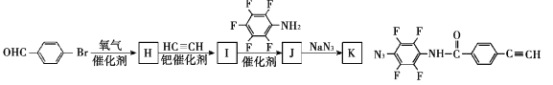
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯的同系物中,有的侧链能被酸性高锰酸钾溶液氧化生成芳香酸,反应如下:
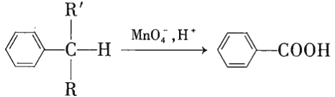 (
(![]() 、
、![]() 表示烃基氢原子)
表示烃基氢原子)
(1)现有苯的同系物甲、乙,分子式都是![]() 。甲不能被酸性高锰酸钾溶液氧化生成芳香酸,则甲的结构简式是_________;乙能被酸性高锰酸钾溶液氧化生成分子式为
。甲不能被酸性高锰酸钾溶液氧化生成芳香酸,则甲的结构简式是_________;乙能被酸性高锰酸钾溶液氧化生成分子式为![]() 的芳香酸,则乙可能的结构有___________种。
的芳香酸,则乙可能的结构有___________种。
(2)有机物丙也是苯的同系物,分子式也是![]() ,它的苯环上的一溴代物只有一种。试写出丙所有可能的结构简式:________。
,它的苯环上的一溴代物只有一种。试写出丙所有可能的结构简式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.![]() 有5种同分异构体
有5种同分异构体
B.某烃的键线式为![]() ,该烃与
,该烃与![]() 按物质的量之比
按物质的量之比![]() 加成时,所得产物有5种
加成时,所得产物有5种
C.相同物质的量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的量相同
D.![]() 分子结构中6个碳原子可能都在一条直线上
分子结构中6个碳原子可能都在一条直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是丁烷(![]() )裂化的实验流程。连接好装置后,需进行的实验操作有:①检查装置的气密性、②排出装置中的空气、③给
)裂化的实验流程。连接好装置后,需进行的实验操作有:①检查装置的气密性、②排出装置中的空气、③给![]() 装置加热等。
装置加热等。![]() 后面的装置以及铁架台等已省略,
后面的装置以及铁架台等已省略,![]() 能将烃氧化成
能将烃氧化成![]() 和
和![]() 是烷烃裂化的催化剂,裂化反应有
是烷烃裂化的催化剂,裂化反应有![]() 。
。


请回答下列问题:
(1)写出甲烷与氧化铜反应的化学方程式:_________________________________。
(2)若对反应后![]() 装置中的混合物(溴水足量)按图2所示流程进行实验:
装置中的混合物(溴水足量)按图2所示流程进行实验:
①分离操作Ⅰ和Ⅱ的名称分别是________、________(填字母);
a.蒸发 b.过滤 c.分液 d.蒸馏
②![]() 溶液的作用是__________________(用离子方程式表示);
溶液的作用是__________________(用离子方程式表示);
③已知B的碳原子数大于A的碳原子数,请写出B的名称:______________________。
(3)假设丁烷完全裂化,流经D、G装置中的气体能完全反应。当E和F装置的总质量比反应前增加了![]() ,G装置的质量比反应前减少了
,G装置的质量比反应前减少了![]() ,则丁烷的裂化产物中甲烷和乙烷的物质的量之比为_______。
,则丁烷的裂化产物中甲烷和乙烷的物质的量之比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】L多巴胺是一种有机物,它可用于帕金森综合症的治疗,其结构简式如下
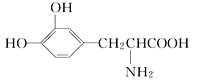
下列关于L多巴胺的叙述不正确的是( )
A. 它属于α氨基酸,既具有酸性,又具有碱性
B. 它遇到FeCl3溶液显紫色
C. 它可以两分子间缩合形成分子式为C18H18O6N2的化合物,该化合物中有3个六元环
D. 它既与酸反应又与碱反应,等物质的量的L多巴胺最多消耗NaOH与HCl的物质的量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有烃的含氧衍生物A(A分子中只有一种官能团),还原A时形成醇B,氧化A时形成酸C。由B、C反应可生成高分子化合物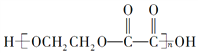 ,下列叙述中错误的是( )
,下列叙述中错误的是( )
A. A属于醛类,其相对分子质量为58,1 mol A与足量的银氨溶液反应可生成4 mol Ag
B. B在一定条件下可通过缩聚反应得到一种新的高聚物
C. 高分子化合物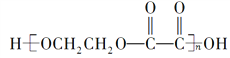 的组成与B、C等物质的混合物的组成相同
的组成与B、C等物质的混合物的组成相同
D. B、C生成高聚物的反应为缩聚反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com