
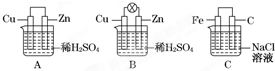
 �۲�ͼA��B��C���ش��������⣺
�۲�ͼA��B��C���ش��������⣺| 0.5mol |
| 0.5L |


 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����һԪ����Һ��pH=1 | ||
| B������Һ��ˮ�����ӻ�����Ϊ1��10-22 | ||
| C������Һ��HA�ĵ����Ϊ 0.1% | ||
D������ˮϡ�ͣ���
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1mol���������1g |
| B��1molCO������Ϊ28g?mol-1 |
| C�������ӵ���������6.02��1023 |
| D��3.01��1023��SO2����Լ��0.5mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��3 | B��7 | C��8 | D��12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��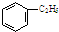 |
B��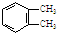 |
C��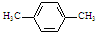 |
D��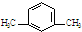 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | HCOOH | HNO2 | H2S | H2SO3 | H2C2O4 |
| ����ƽ�ⳣ�� ��25�棩 | K=1.8��10-4 | K=5.1��10-4 | K1=9.1��10-8 K2=1.1��10-12 | K1=1.23��10-2 K2=6.6��10-8 | K1=5.4��10-2 K2=5.4��10-5 |
| A�� | HNO2+HS-�TNO2-+H2S�� |
| B�� | 2HCOOH+SO32-�T2HCOO-+H2O+SO2�� |
| C�� | H2SO3+2HCOO-�T2HCOOH+SO32- |
| D�� | H2SO3+SO32-�T2HSO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
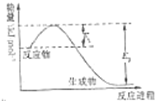 ���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯����������������������Ҫ���ã���ش��������⣺
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯����������������������Ҫ���ã���ش��������⣺| t/�� | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| PH | 6.5��8.5 |
| Ca2+��Mg2+��Ũ�� | ��0.0045mol/L |
| ϸ������ | ��100��/mL |

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com