
 NA×一个分子中含有的氧原子数目;
NA×一个分子中含有的氧原子数目; NA×一个分子中含有的中子数目来计算.
NA×一个分子中含有的中子数目来计算.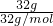 NA×2=2NA个,32g的臭氧中含有的氧原子数=
NA×2=2NA个,32g的臭氧中含有的氧原子数=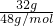 NA×3=2NA个,所以32gO2与O3的混合物中含有2NA个氧原子,故B错误;
NA×3=2NA个,所以32gO2与O3的混合物中含有2NA个氧原子,故B错误; NA×一个分子中含有的中子数目=
NA×一个分子中含有的中子数目=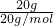 NA×10=10NA,故D正确.
NA×10=10NA,故D正确.

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com