
【题目】实验室中要配制0.1mol·L-1的纯碱溶液950ml,配制时应选用的容量瓶的规格和称取的纯碱质量分别是
A.950mL 10.1g B.1000mL 10.6g C.1000mL4.0g D.任意规格,4.0g
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】含有MgCl2、NaCl、Na2SO4三种物质的混合溶液,其中含有Cl-为1.8mol,Na+为2mol,Mg2+为0.5mol,则SO42-的物质的量为
A.0.6mol B.0.7mol C.1.2mol D.1.0mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的叙述不正确的是( )
A. 甲烷、甲苯、乙醇、乙酸都可以发生取代反应
B. 煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏制取
C. 乙酸乙酯在无机酸或碱存在时都能发生水解反应
D. 淀粉、纤维素、蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活关系密切,请从现有下列五种物质选择填空:
A.葡萄糖 B.抗酸药(氢氧化铝) C.麻黄碱 D.阿司匹林 E.青霉素
(1)具有解热镇痛作用,用于治疗感冒的是____。
(2)对支气管哮喘症有明显疗效的是 _____。
(3)_____是最重要的抗生素,在注射之前,需要进行皮肤敏感试验。
(4)治疗胃酸过多,应该选择 ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:

(1)写出AlCl3与氨水反应的化学反应方程式_________________________。
(2)判断流程中沉淀是否洗净所用的试剂是 ,高温焙烧时,用于盛放固体的仪器名称是 。
Ⅱ、无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。

(3)其中装置A用来制备氯气,写出其离子反应方程式:______________________。
(4)装置B中盛放饱和NaCl溶液,该装置的主要作用是__________________________。
(5)F中试剂是________。G为尾气处理装置,其中反应的化学方程式:__________________。
(6)制备氯气的反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:与足量AgNO3溶液反应,称量生成的AgCl质量。此方案 (填“可行”,“不可行”),理由是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg和Al的混合物投入500 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。则下列说法正确的是( )

A.Mg和Al的总质量为8 g
B.原稀硫酸溶液的物质的量浓度为5 mol·L-1
C.生成的H2在标准状况下的体积为11.2 L
D.NaOH溶液的物质的量浓度为5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠等等,这些物质在实际生活中有广泛的应用,一定条件下相互间能进行转化。完成下列计算:
(1)将7.8 g Na2O2完全溶于93.8 g水中,所得溶液中溶质的质量分数为________。
(2)将11.6 g二氧化碳和水蒸气的混合物与足量的Na2O2充分反应,固体质量增加了3.6 g,则原混合气体的平均相对分子质量为________。
(3)向100 mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M(不含结晶水)。通入二氧化碳的体积V(标准状况下)与M的质量W的关系如下图所示。

(a)推断b点时M的组成成分___________________。(填化学式,下同)
(b)若向b点的盐溶液中只加入0.03 mol某钠的化合物,充分反应后,减压低温蒸发得到无水Na2CO3 8.48 g,则加入的物质可以是________或________。
(4)将31 g NaOH和NaHCO3的固体混合物,在密闭容器中加热到250 ℃,经充分反应后排出气体、冷却,称得剩余固体的质量为N g,试分析不同N值时,剩余固体的组成成分(已知NaHCO3的分解温度低于250 ℃)__________ ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟生成E,A是强碱,D是海水中浓度最高的盐(部分反应物和生成物及水已略去)。
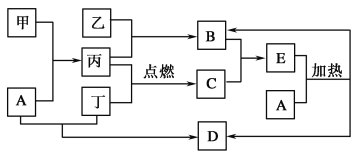
请回答下列问题:
(1)写出乙与丙生成B的反应条件:________________。
(2)写出甲和A溶液反应的离子方程式:______________。
(3)检验E中的阳离子时,取少量E于试管中, 则证明E中有该阳离子。
(4)写出实验室制取B的化学方程式:________________。
(5)B常见用途:_______________、_______________、_______________。
(6)常用作工业制某酸的原料,写出由B制该酸过程中的化学方程式:
______________________、 、________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象中,纵坐标为沉淀物的量,横坐标为溶液中加入反应物的物质的量,试按题意将图象中相应的数字序号填入表中的顺序为
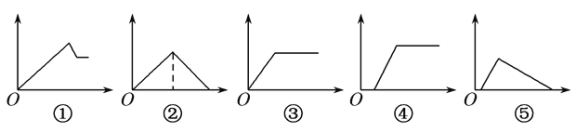
溶液 | 加入物质 | 相应序号 |
(1)氯化铝溶液 | 加入过量氨水 | |
(2)饱和澄清石灰水 | 通入过量CO2气体 | |
(3)含少量NaOH的偏铝酸钠溶液 | 通入过量CO2气体 | |
(4)含少量NaOH的偏铝酸钠溶液 | 逐滴加入稀盐酸 | |
(5)MgCl2、AlCl3的混合溶液 | 逐滴加入NaOH溶液至过量 |
A. ①③②④⑤ B. ③⑤④②①
C. ①②③④⑤ D. ③②④⑤①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com