
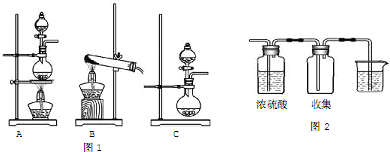
分析 (1)实验室中用乙醇制取乙烯气体,需要用温度计控制反应温度,图示装置中缺少温度计;
(2)浓氨水与生石灰不需要加热即可制备少量氨气,其原理是:浓氨水易挥发出氨气,氧化钙溶于水生成氢氧化钙,并放出大量的热,氢氧根浓度增大,有利于氨气生成,放出大量的热,有利于氨气逸出;
(3)B装置适合固体加热制备气体,C装置适合固体与液体不需要加热制备气体;
(4)发生装置符合固体与液体加热制备气体,可以用浓硫酸进行干燥,利用向上排空气法收集,所制备气体密度比空气大,可以用二氧化锰与浓盐酸在加热条件下制备氯气,烧杯中溶液吸收氯气,防止污染空气,可以盛放氢氧化钠溶液,制备的氯气中含有HCl,用饱和食盐水除去HCl.
解答 解:(1)实验室中用乙醇制取乙烯气体,需要用温度计控制反应温度,把装置A中双孔塞换成三孔塞,增加一支温度计并插入反应液面下,
故答案为:把装置A中双孔塞换成三孔塞,增加一支温度计并插入反应液面下;
(2)浓氨水与生石灰不需要加热即可制备少量氨气,可以选用C装置制备,其原理是:浓氨水易挥发出氨气,氧化钙溶于水生成氢氧化钙,并放出大量的热,氢氧根浓度增大,有利于氨气生成,放出大量的热,有利于氨气逸出,与氢氧化钙溶解度无关,
故答案为:C;B;
(3)现有两种方法制取氧气,可供选用的药品有:KClO3、Na2O2、NaOH、H2O、Na2CO3、MnO2;若选装置B,适合固体加热制备气体,需选用的试剂为KClO3、MnO2,氯酸钾在二氧化锰作催化剂条件下反应生成氯化钾和氧气;若选装置C,合固体与液体不需要加热制备气体,需选用的试剂可以为H2O2、MnO2,过氧化氢分解得到水与氧气,
故答案为:KClO3、MnO2; H2O2、MnO2;
(4)若把装置图1中的A与图2相连,浓硫酸只能干燥酸性气体,该装置不能制取氨气;实验室制取二氧化碳不需要加热,应用向下排空气法收集氢气,可制取的气体为②Cl2 ,反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+MnCl2+2H2O,小烧杯中液体用于吸收多余氯气,防止污染空气,可以是氢氧化钠溶液,制备的氯气中含有HCl,为了获得较纯净的产物,应在A与“图2”间增加盛有饱和食盐水的洗气瓶,除去氯气中的HCl,
故答案为:②;MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+MnCl2+2H2O;NaOH;盛有饱和食盐水的洗气瓶.
点评 本题考查常见气体的制备原理及装置的选择,题目难度中等,明确常见气体的性质及实验室制法为解答本题的关键.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
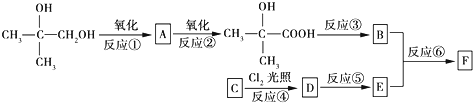
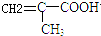 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$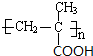 .
.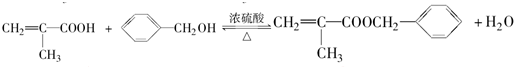 .
.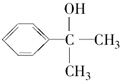 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
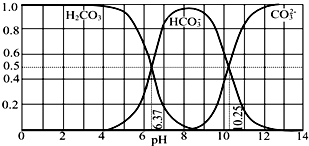
| A. | pH=10.25时,c(Na+)═c(CO32-)+c(HCO3-) | |
| B. | 为获得尽可能纯的NaHCO3,宜控制溶液的pH为7~9之间 | |
| C. | 根据图中数据,可以计算得到H2CO3第一步电离的平衡常数K1(H2CO3)=10-6.37 | |
| D. | 若是0.1mol NaOH 反应后所得的1L溶液,pH=10时,溶液中存在以下关系:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 1:l | C. | 1:2 | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用大理石和稀盐酸反应制CO2:CO32-+2H+═CO2↑+H2O | |
| B. | Cl2通入石灰乳中:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 氢氧化钠溶液腐蚀玻璃:2OH-+SiO2═SiO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用甲图装置电解精炼镁 | |
| B. | 用乙图装置验证试管中铁丝发生析氢腐蚀 | |
| C. | 用丙图装置构成铜锌原电池 | |
| D. | 用丁图装置对充电电池进行充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:D>B>C>A | |
| B. | 金属性:B>C | |
| C. | A、D最高化合价与最低化合价的代数和分别为0和6 | |
| D. | B和A、C形成的氧化物均不反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com