
分析 已知:①.C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol,
②.2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol,
③.CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ/mol,
根据盖斯定律,①-②×$\frac{1}{2}$-③可得:C(s)+H2O(g)═CO(g)+H2(g),反应热也进行相应计算.
解答 解:已知:①.C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol,
②.2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol,
③.CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ/mol,
根据盖斯定律,①-②×$\frac{1}{2}$-③可得:C(s)+H2O(g)═CO(g)+H2(g),
故△H=-393.5kJ/mol-(-483.6kJ/mol)×$\frac{1}{2}$-(-283kJ/mol)=+131.3 kJ/mol,
故答案为:+131.3 kJ/mol.
点评 本题考查运用盖斯定律计算反应热,难度不大,关键是根据已知热化学方程式构造出目标热化学方程式.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 向 0.1 mol/L的氨水中加少量硫酸铵固体,则溶液中$\frac{c(O{H}^{-})}{(N{H}_{3}•{H}_{2}O)}$增大 | |
| B. | 常温下,0.1 mol/L一元酸(HA)溶液的 pH=3,则该溶液中,c2(H+)=c(H+)×c(A-)+Kw | |
| C. | 向含有 1 mol KAl(SO4)2 的溶液中加入 Ba(OH)2 溶液得到沉淀的物质的量最多为 2 mol | |
| D. | 将 Ca(ClO)2、Na2SO3、FeCl3、NaAlO2 溶液蒸干均得不到原溶质 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
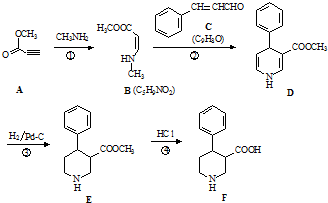
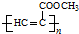 .
.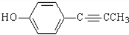 .
.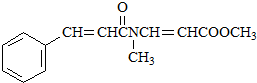 .
.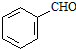 、CH3CH2OH和
、CH3CH2OH和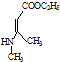 为原料,合成
为原料,合成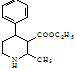 ,写出合成流程图(无机试剂任用).
,写出合成流程图(无机试剂任用).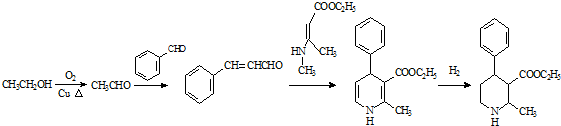
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
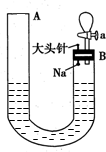 如图是有关钠与水反应及产物检验的实验装置.实验开始时先向管内加入滴有酚酞的水,使水位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时Na掉入水中.回答下列问题:
如图是有关钠与水反应及产物检验的实验装置.实验开始时先向管内加入滴有酚酞的水,使水位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时Na掉入水中.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳原子数≤10 的烷烃,其一氯代物没有同分异构体的烷烃共有3种 | |
| B. | 烯烃、炔烃、芳香烃都能与溴水反应而使其褪色 | |
| C. | 等质量的CH≡CH和C6H6完全燃烧时消耗等物质的量的氧气 | |
| D. | 分子式为C6H12与C3H6的两种烃一定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | T℃时,向NaCl和NaBr的混合 溶液中滴加AgNO3溶液 | 先出现白色沉淀 | T℃时,Ksp: AgCl<AgBr |
| B | 向等浓度的Na2CO3溶液或Na2SO4 溶液中滴加酚酞试剂 | Na2CO3溶液变红色,Na2SO4 溶液无明显现象 | 非金属性:S>C |
| C | 常温下,取饱和CaSO4溶液或醋酸 溶液做导电性实验 | 醋酸实验的灯泡较亮 | CaSO4和醋酸均 为弱电解质 |
| D | 向品红溶液中滴加NaClO溶液 或通入SO2气体 | 品红溶液均褪为无色 | 两者均有漂白性 且原理相同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com