
| 18 |
| 16 |
| ||
| ||


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
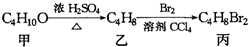 ,丙的结构简式不可能是( )
,丙的结构简式不可能是( )| A、CH3CH(CH2Br)2 |
| B、(CH3)2CBrCH2Br |
| C、C2H5CHBrCH2Br |
| D、CH3(CHBr)2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
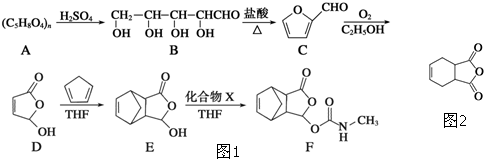
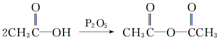 化合物G(结构如图2所示)是合成抗病毒药阿昔洛韦的中间体.请写出以OHCCH(Br)CH2CHO和1,3-丁二烯为原料制备G的合成路线流程图2(无机试剂任用).合成路线流程图示例如下:H2C=CH2
化合物G(结构如图2所示)是合成抗病毒药阿昔洛韦的中间体.请写出以OHCCH(Br)CH2CHO和1,3-丁二烯为原料制备G的合成路线流程图2(无机试剂任用).合成路线流程图示例如下:H2C=CH2| HBr |
| NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
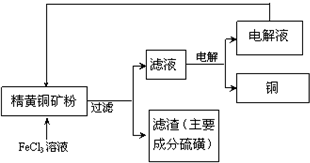 工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺.
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺.查看答案和解析>>
科目:高中化学 来源: 题型:

| NaNO2 |
| ①O3 |
| ②Zn/H2O |
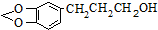 是一种合成药物的中间体,以CH2(COOH)2、CH2Cl2 及
是一种合成药物的中间体,以CH2(COOH)2、CH2Cl2 及 (无机试剂任用)为原料制备该化合物,请将合成该化合物路线流程图补充完整.
(无机试剂任用)为原料制备该化合物,请将合成该化合物路线流程图补充完整.| 反应试剂 |
| 反应条件 |
| 反应试剂 |
| 反应条件 |
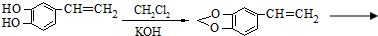
查看答案和解析>>
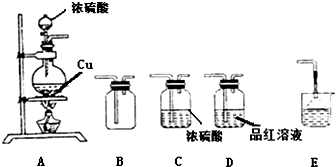
科目:高中化学 来源: 题型:
| 编号 | A | B | C |
| 发生装置 |  |  | 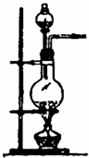 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com