


科目:高中化学 来源:不详 题型:单选题

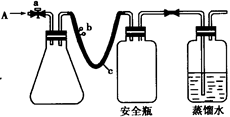
| A.利用①可以制取乙烯 | B.装置②可配制一定物质的量浓度的稀硫酸 |
| C.利用③可以进行中和热测定 | D.利用④可以进行草酸晶体的分解实验 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.SO2、H2S、Cl2 | B.SO2、O2、NH3 |
| C.SO2、CO2、O2 | D.HCl、H2S、HI |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
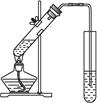
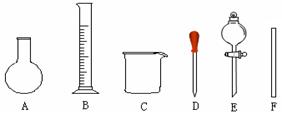
| A.用量筒准确量取所需的浓硫酸,沿玻璃棒倒入盛有适量水的烧杯中。并用玻璃棒不断搅拌至冷却 |
| B.将烧杯中的硫酸沿玻璃棒注入所选的容量瓶中① |
| C._______________________________________________________________________ |
| D.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2 cm 处 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
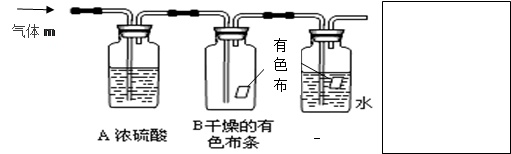
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 实验内容 | 实验现象 |
| A | 收集一集气瓶气体,观察颜色,然后向瓶内倒入约占瓶容积1/5的蒸馏水,充分振荡。 | 蒸馏水呈浅黄绿色,瓶内气体仍呈黄绿色。 |
| B | 取出瓶内部分溶液,滴入紫色石蕊试液中直至过量。 | 紫色石蕊试液先变红色,后红色褪色。 |
| C | 取出瓶内剩下的部分溶液,滴入硝酸银溶液中。 | 产生大量白色沉淀 |
| D | 最后向瓶内倒入少量浓氢氧化钠溶液,振荡。 | 瓶内黄绿色气体立即消失。 |
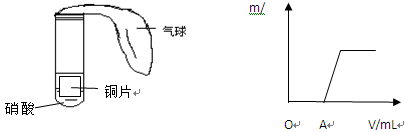
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com