
下列叙述正确的是
①配位键在形成时,是由成键双方各提供一个电子形成共用电子对
②价电子排布式为ns2的原子属于ⅠA或ⅡA族元素
③Ge是ⅣA族的一个主族元素,其核外电子排布式为Ge:[Ar]4s24p2,属于P区元素
④非极性分子往往是高度对称的分子,比如BF3,PCl5,H2O2,CO2这样的分子
⑤化合物NH4Cl和CuSO4·5H2O都存在配位键
⑥AgCl是一种白色的沉淀,不溶于硝酸、浓硫酸、烧碱溶液,却能溶于氨水中
⑦熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、非电解质、盐、分子晶体
⑧氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水
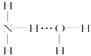 的性质可知NH3·H2O的结构式为
的性质可知NH3·H2O的结构式为
①③ B.②③ C.⑤⑥ D.④⑤
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
为了探究几种气态氧化物的性质,某同学设计了如图所示的一组实验:用三个集气瓶收集满SO2、NO2,然后分别倒置于盛有水的水槽中;分别缓慢通入适量O2或Cl2;一段时间后,装置A、B的集气瓶中充
满溶液,装置C的集气瓶中还有气体剩余。
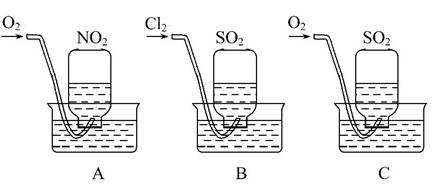
(1)写出装置A中总反应的化学方程式___________________________。
(2)实验前,在装置C的水槽里滴加几滴紫色石蕊溶液,观察到的现象是_______
______________________________________________,通入氧气后,可观察到的现象是_____________________________________________________,写出发生反应的总化学方程式______________________________________________。
(3)装置B中,溶液充满集气瓶后,在水槽里滴加适量的Ba(NO3)2溶液,可观察到的现象为_____________________________________,写出有关反应的离子方程式_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列说法正确的是:( )
A.2 mol·L-1 的Na2SO4溶液中含有4NA个Na+
B.18克水所含的电子数为10NA
C.在标准状况下,11.2L氖气中含有NA个氖原子
D.NA个水分子的相对分子质量之和等于水的摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素周期表和元素周期律的说法,错误的是
① 元素周期表中s区、d区和ds区的元素都是金属元素
② d区元素最后一个核外电子一定填充在s能级上
③ 原子核外电子的能层越多,原子半径越大
④ 同一周期自左至右,元素的第一电离能依次增大
A. 只有①②③ B. 只有②③ C. 只有③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中元素均为中学化学常见短周期元素根据表中信息,下列说法不正确的是
A.X和W形成的化合物是共价化合物 B.常温下单质与水反应速率X大于N
C.最高价氧化物对应水化物酸性W大于Z
D.X和Y的单质在一定条件下反应可生成一种淡黄色的固体化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示各物质是由1~20号元素中部分元素组成的单质或其化合物,
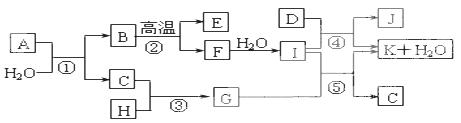 图中部分反应条件未列出。已知C、H是无色有刺激性气味的气体,D是一种黄绿色的气体单质,物质J可用于饮水消毒。反应②和④是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法。
图中部分反应条件未列出。已知C、H是无色有刺激性气味的气体,D是一种黄绿色的气体单质,物质J可用于饮水消毒。反应②和④是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法。
请回答下列问题:
(1)用电子式表示H的形成过程 ;
(2)写出E溶液与过量I溶液反应的离子方程式 。
(3)实验室还可用C的浓溶液与F制备气体C,反应理由是 。
(4)物质A由三种元素组成,1 mol A与水反应可生成1 mol B和2 mol C,A化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
人类活动对自然界中氮循环和环境的影响。
(1)氮氧化物是形成________和________的一个重要原因。
(2)光化学烟雾是指______________________________________________________。
(3)大气中氮氧化物主要来源于____________________________________________。
(4)氮的水体污染:进入水体的氮的含量增大,会导致藻类“疯长”,迅速地覆盖在水面上,造成水体的________。
查看答案和解析>>
科目:高中化学 来源: 题型:
按照下列实验方法制备气体,既合理又实用的是(双选)( )
A.锌粒与稀硝酸反应制备氢气
B.向浓盐酸中滴加浓硫酸制备HCl
C.Na2SO3与硫酸反应制备SO2
D.大理石与稀硫酸反应制备CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化铝广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应
Al2O3+N2+3C 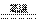 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com