
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一。镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标。某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案:
方案一:取三块镀锌铁皮(A、B、C,截自同一块镀锌铁皮),将镀锌铁皮A放入烧杯中,加入40 mL 6 mol·L-1盐酸,反应时用玻璃棒小心翻动镀锌铁皮,待锌镀层反应完全时,立即将未反应的铁皮取出,洗涤、小心烘干、称量。将B、C重复上面的实验。
(1)锌镀层完全反应的标志是
________________________________________________________________________。
(2)如何检验铁片已经洗净
________________________________________________________________________
________________________________________________________________________。
(3)该小组的实验数据记录及数据处理如下,完成下列表格。(锌的密度为7.14 g/cm3)
|
|
数据记录 |
数据处理 |
||||
|
镀锌铁皮 |
长度/cm |
宽度/cm |
镀锌铁皮质量/g |
铁皮质量/g |
锌镀层厚度(单侧)/cm |
锌镀层平均厚度(单侧)/cm |
|
A |
5.00 |
4.90 |
4.460 |
4.313 |
4.201×10-4 |
|
|
B |
5.10 |
5.00 |
4.421 |
4.267 |
4.229×10-4 |
|
|
C |
5.20 |
5.00 |
4.640 |
4.467 |
4.660×10-4 |
计算镀锌铁皮锌镀层平均厚度(单侧)________cm。本实验中产生误差的地方可能有哪些(任意列举两
种)________________________________________________________________________
________________________________________________________________________、
________________________________________________________________________。
方案二:已知锌与强碱溶液反应的离子方程式为:Zn+2OH-+2H2O===[Zn(OH)4]2-+H2↑。某同学按下图装置设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S cm2、质量为m g的镀锌铁皮放入6 mol·L-1 NaOH溶液中。回答下列问题。

(4)装置中导管a的作用是
________________________________________________________________________
________________________________________________________________________。
(5)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②待B中不再有气体产生并恢复至室温;③由A向B中滴加足量NaOH溶液;④上下移动C,使干燥管和C中液面相平。上述操作的顺序是
____________________________________________________(填序号)。
(6)实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL(实验条件下的气体摩尔体积为Vm L·mol-1)。则镀锌铁皮的厚度为
________________________________________________________cm。(写出数学表达式)
(1)产生气泡的速率突然减小
(2)取最后一次洗涤液,加入AgNO3溶液,若无白色沉淀生成,则铁片已洗净(或用玻璃棒蘸取最后一次洗涤液,滴在蓝色石蕊试纸上,若不变红色,则铁片已洗净)
(3)4.215×10-4 镀锌铁皮长、宽测量;反应前后铁皮质量称量;终点判断;反应后铁皮洗涤;铁皮烘干程度(任选两个)
(4)使分液漏斗和锥形瓶内气压相同,以便于NaOH溶液能顺利滴下
(5)④①③②④①(回答④①③②也可)
(6)h=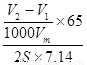
【解析】
试题分析:(1)当锌镀层完全反应后就是铁与盐酸反应,由于锌和铁的活泼性不同,反应速率就不同。
(2)从溶液中取出的铁片必然带有盐酸及其盐,当洗净时也就是不再含有盐酸及其盐,所以检验铁片是否洗净就是检验氯离子,也可检验其酸性。
(3)由三组所列锌镀层厚度数据来看,第三组数据与另两组有较大差距,应舍去,取前两组数据取平均值得4.215×10-4 cm;本实验中产生误差的地方可能有:长度和宽度的测量,质量的测量,恰好反应的判断,反应后铁皮的洗涤是否干净、烘干是否彻底等。
(4)随着分液漏斗内的液体不断流下,其内部压强变小,不利于液体流下。
(5)本实验的关键是测量气体的体积。根据此装置的原理,应两次记录C中的读数,取其差值就是所得气体的体积,所以第一步就应该是④。
(6)V(H2)=(V2-V1) mL,n(Zn)=n(H2)=(V2-V1)/(1000·Vm),m(Zn)=65 g·mol-1n(Zn),锌的密度是7.14 g·cm-3,V(Zn)=m(Zn)/7.14,由于铁片表面有上、下两层,所以每一层的厚度h=V(Zn)/2S,代入即得答案。
考点:考查化学实验的设计、分析与评价
点评:化学是一门以实验为基础的学科,所以有化学实验即科学探究之说法。纵观近几年高考,主要以考察探究性实验和物质制备实验为主。这些探究性和制备性实验的试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论,有利于培养学生的综合实验能力,提升学生的科学素养。


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:阅读理解
 “白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一.镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标.某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案:
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一.镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标.某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案:
| ||
| 2S×7.14 |
| ||
| 2S×7.14 |
查看答案和解析>>
科目:高中化学 来源:2012届吉林省吉林一中高三上学期期末质量检测化学试卷 题型:实验题
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一。镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标。某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实 验方案:
验方案:
方案一:取三块镀锌铁皮(A、B、C,截自同一块镀锌铁皮),将镀锌铁皮A放入烧杯中,加入40mL 6mol·L—1盐酸,反应时用玻璃棒小心翻动镀锌铁皮,待锌镀层反应完全时,立即将未反应的铁皮取出,洗涤、小心烘干、称量。将B、C重复上面的实验。
(1)锌镀层完全反应的标志是 。
(2)如何检验铁片已经洗净
。
方案二:已知锌与强碱溶液反应的离子方程式为:Zn+2OH—+2H2O=[Zn(OH)4]2—+H2↑。某同学按右图装置设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S cm2、质量为mg的镀锌铁皮放入6mol·L—1 NaOH溶液中。回答下列问题:
(3)装置中导管a的作用是 。
(4)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;②待B中不再有气体产生并恢复至室温;③由A向B中滴加足量NaOH溶液;④上下移动C,使干燥管和C中液面相平。
上述操作的顺序是 (填序号)。
(5)实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL(已知Zn的密度为7.14g/cm3,实验条件的气体摩尔体积为Vm L / mol)。则镀锌铁皮的镀层厚度为 cm。(写出数学表达式)
查看答案和解析>>
科目:高中化学 来源:浙江省期末题 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
“白铁皮”具有较强的耐腐蚀性,是生产中常用的金属材料之一。镀锌层犹如铁皮的保护层,这层膜的厚度及均匀度也成了判断镀层质量的重要指标。某研究性学习小组为了测定镀锌铁皮的厚度,设计了下面的实验方案:
方案一:取三块镀锌铁皮(A、B、C,截自同一块镀锌铁皮),将镀锌铁皮A放入烧杯中,加入40mL 6mol?L―1盐酸,反应时用玻璃棒小心翻动镀锌铁皮,待锌镀层反应完全时,立即将未反应的铁皮取出,洗涤、小心烘干、称量。将B、C重复上面实验。
![]()
(1)锌镀层完全反应的标志是 。
![]()
(2)如何检验铁片已经洗净 。
![]()
(3)该小组的实验数据记录及数据处理如下,完成下列表格(锌的密度为7.14g/cm3)
| 数据记录 | 数据处理 | ||||
镀锌铁皮 | 长度
| 宽度
| 镀锌铁皮质量/g | 铁皮
| 锌镀层厚度
| 锌镀层平均厚度(单侧)/cm |
A | 5.00 | 4.90 | 4.460 | 4.313 | 4.201×10―4 |
|
B | 5.10 | 5.00 | 4.421 | 4.267 | 4.229×10―4 | |
C | 5.20 | 5.00 | 4.640 | 4.467 | 4.660×10―4 | |
计算镀锌铁皮锌镀层平均厚度(单侧) cm。本实验中产生误差的原因可能有哪些(任意例举两种) 、
方案二:已知锌与强碱溶液反应离子方程式为:Zn+2OH―+2H2O=[Zn(OH)4]2―+H2↑。某同学按右图装置设 计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S cm2、质量为m g的镀锌铁皮放入6mol?L―1 NaOH溶液中。回答下列问题:
计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S cm2、质量为m g的镀锌铁皮放入6mol?L―1 NaOH溶液中。回答下列问题:
(4)装置中导管a的作用是 。
(5)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②待B中不再有气体产生并恢复至室温;③由A向B中滴加足量NaOH溶液;④上下移动C,使干燥管和C中液面相平。上述操作的顺序是 (填序号)。
(6)实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL(实验条件的气体摩尔体积为Vm mol?L―1)。则镀锌铁皮的厚度为 cm。(写出数学表达式)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com