

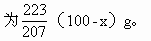
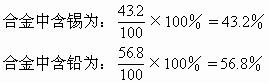
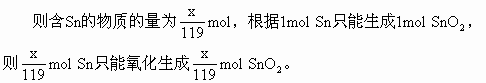
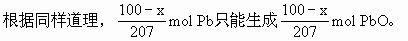



| 解得 x=43.2(g) | (锡的质量) |
| 100-x=56.8(g) | (铅的质量) |



科目:高中化学 来源:不详 题型:单选题
| A.单质都是无色晶体 |
| B.单质中硅单质熔点最高 |
| C.碳族元素形成的化合物种类最多 |
| D.在化合物中最稳定的化合价都是+4价 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钠与水反应:2Na+2 H2O = 2Na+2OH-+H2↑ |
| B.氧化钠与盐酸:O2-+2H+ = H2O |
| C.碳酸氢钠与稀硫酸: CO32-+2H+=H2O+CO2↑ |
| D.烧碱溶液与碳酸氢钠溶液:HCO3-+OH-= H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
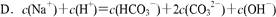
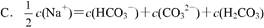
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
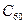 ,首次制成了“纳米车”(如图.每辆“纳米车”是用一个有机分子和4个球形笼状分子“组装”而成。“纳米车”可以用来运输单个的有机分子,生产复杂的材料和药物,成为“纳米生产”中的有用工具。下列说法正确的是
,首次制成了“纳米车”(如图.每辆“纳米车”是用一个有机分子和4个球形笼状分子“组装”而成。“纳米车”可以用来运输单个的有机分子,生产复杂的材料和药物,成为“纳米生产”中的有用工具。下列说法正确的是


A.我们可以直接用肉眼清晰地看到这种“纳米车”的运动 |
B.“纳米车”的诞生,说明人类操纵分子的技术进人一个新阶段 |
C.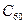 是一种新型化合物 是一种新型化合物 |
D.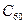 熔点比金刚石熔点高 熔点比金刚石熔点高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题









查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.同系物 | B.同分异构体 | C.同素异形体 | D.同位素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.两种分子的中心原子的杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 |
| D.氨气分子是极性分子而甲烷是非极性分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com