
��ѧ�ҷ��֣�ʳ��Ϻ���ˮ�����ද���ͬʱ����ά����C�����ж���������Ϊ����������+5�����������ά����C�������£��ܹ�ת��Ϊ�ж���+3�۵ĺ��黯���ͨ��������Ϣ��գ�
��1��ά����C���� ��������ԡ���ԭ�ԡ�����
��2������������+5������������Ϊ �������������ԭ��������+5����Ԫ�ط��� ��Ӧ�����������ԭ������2mol +5������ȫת��Ϊ +3���飬��ת�� �����ӣ���NA��ʾ�����ӵ���������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�����ɹŰ�ͷ�ھ���ѧ���������п������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��100mL0.1mol��L-1��立�[NH4Al(SO4)2•12H2O]��ˮ��Һ�У���ε���0.1mol��L-1��Ba(OH)2��Һ�����ó�����������Ba(OH)2��Һ�����������ͼ��ʾ[��֪Ba(AlO2)2��������]������˵����ȷ���ǣ� ��
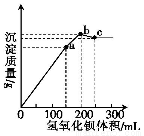
A��a����Һ�д������ڵ�������NH4+��SO42��
B��b����Һ��c(NH3��H2O)ԼΪ0.1mol��L-1
C��a��b�����У���Ӧ��ֻ��SO42��
D��b��c�����У���Ӧ����Al(OH)3��NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������人�ڶ���ѧ�߶������п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪ij�¶���CH3COOH��NH3��H2O�ĵ��볣����ȣ�����10 mLŨ��Ϊ0.1 mol��L��1��CH3COOH��Һ�еμ���ͬŨ�ȵİ�ˮ���ڵμӹ����У� ��
A��ˮ�ĵ���̶�ʼ������
B��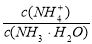 �������ټ�С
�������ټ�С
C��c(CH3COOH)��c(CH3COO��)֮��ʼ�ձ��ֲ���
D�������백ˮ�����Ϊ10 mLʱ��c (NH4��)=c(CH3COO��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ���ˮ������ѧ��һ���¿�������ѧ���������棩 ���ͣ�ѡ����
ͬ��ͬѹ�£�������ͬ������κ������к��еķ�������ͬ����һ���¶Ⱥ�ѹǿ�£�10�������A2��30�������B2��������20���ij����C��������C�Ļ�ѧʽΪ �� ��
A�� AB B�� A2B C�� AB3 D�� AB2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ���ˮ������ѧ�߶����¿�����ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ���ǣ� ��
A��0.2 mol/L CH3COONa��Һ��0.1 mol/L HCl��Һ�������Ϻ���Һ�����ԣ�
c��CH3COO������c��Na������c��Cl������c��H������c��OH����
B��pH��3�������NaNO3�Ļ����Һ�У�c��Na������c��Cl����
C��0.1 mol/L NaHCO3��Һ�У�c��Na������c��H������c��HCO3-����c��CO32-����c��OH����
D�����ʵ���Ũ����ȵ�HCN�����ᣩ��NaCN��Һ�������Ϻ��У�
c��HCN����2c��H������2c��OH������c��CN����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣������һ�и�һ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ʵ��������Ҫ0.2 mol��L-1��CuSO4��Һ950 mL������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�ȡ�������壨CuSO4��5H2O���������ֱ���
A��950 mL 30.4 g B��950 mL 47.5g
C��1000 mL 50.0 g D��1000 mL 32.0g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣������һ�и߶������п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з���ʽֻ�ܱ�ʾһ�����ʵ���
A��C3H4Cl2 B��CH4O C��C2H6O D��C2H4O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ�߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������Һ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ��Na2S2O3+H2SO4=Na2SO4+SO2+S��+H2O,���и���ʵ�������ȳ��ֻ��ǵ���
ʵ�� | ��Ӧ�¶�/�� | Na2S2O3��Һ | ϡH2SO4 | H2O | ||
V/mL | c/��mol��L-1�� | V/mL | c/��mol��L-1�� | V/mL | ||
A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
B | 25 | 6 | 0.2 | 5 | 0.2 | 9 |
C | 35 | 8 | 0.15 | 10 | 0.1 | 2 |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶���ѧ�����У�������ѧ�Ծ��������棩 ���ͣ�ѡ����
ij������ķ����������£�c(NH4+)��2.0��10��5 mol��L��1��c(Cl��)��6.0��10��5 mol��L��1��c(Na��)��1.9��10��5 mol��L��1��c(NO3��)��2.3��10��5 mol��L��1��c(SO42��)��2.8��10��5 mol��L��1����˴������pH��ԼΪ
A��3 B��4 C��5 D��6
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com