
一定温度下,反应2SO2(g)+O2(g)  2SO3(g),达到平衡时,n(SO2)∶n(O2)∶n(SO3)=2∶3∶4。缩小体积,反应再次达到平衡时,n(O2)=0.8 mol,n(SO3)=1.4 mol,此时SO2的物质的量应是
2SO3(g),达到平衡时,n(SO2)∶n(O2)∶n(SO3)=2∶3∶4。缩小体积,反应再次达到平衡时,n(O2)=0.8 mol,n(SO3)=1.4 mol,此时SO2的物质的量应是
( )。
A.0.4 mol B.0.6 mol C.0.8 mol D.1.2 mol
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
食盐(NaCl)是生活中常用的调味品,HCl是胃酸的主要成分,下列关于两种物质的说法正确的是
( )。
A.炒菜时放入食盐并不破坏NaCl中的化学键
B.HCl的电子式是H+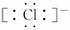
C.NaCl熔化时破坏共价键
D.HCl的结构式是H—Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
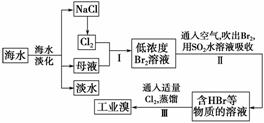
(1)请列举海水淡化的两种方法:________、________。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_________。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_______,
由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_______。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:

请你参与分析讨论:
①图中仪器B的名称是____________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?___________。
④C中液体颜色为________________。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,可逆反应2A
 B+3C,在下列四种状态中,处于平衡状态的是
B+3C,在下列四种状态中,处于平衡状态的是
( )。
| 正反应速率 | 逆反应速率 | |
| A | vA=2 mol·L-1·min-1 | vB=2 mol·L-1·min-1 |
| B | vA=2 mol·L-1·min-1 | vC=2 mol·L-1·min-1 |
| C | vA=1 mol·L-1·min-1 | vB=2 mol·L-1·min-1 |
| D | vA=1 mol·L-1·min-1 | vC=1.5 mol·L-1·min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下列反应中,属于放热反应的是________,属于吸热反应的是________。
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)用铜、银与硝酸银设计一个原电池,此电池的负极是________,负极的电极反应式是_________________________________________________。
(3)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了3.25 g,铜表面析出了氢气________L(标准状况),导线中通过________mol电子。
(4)某化学反应,设反应物的总能量为E1,生成物的总能量为E2,若E1>E2,则该反应为________热反应,该反应过程可以看成________________________________________________________________。
中和反应都是________热反应,其实质是__________________________________________________________________
________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z三种主族元素的单质在常温下都是常见的无色气体,在适当条件下,三者之间可以两两发生反应生成分别是双核、三核和四核的甲、乙、丙三种分子,且乙、丙分子中含有X元素的原子个数比为2∶3。请回答下列问题:
(1)元素X的名称是________,丙分子的电子式为________。
(2)若甲与Y单质在常温下混合就有明显现象,则甲的化学式为________。丙在一定条件下转化为甲和乙的反应方程式为___________________________。
(3)化合物丁含X、Y、Z三种元素,丁是一种常见的强酸,将丁与丙按物质的量之比1∶1混合后所得物质戊的晶体结构中含有的化学键为________(选填序号)。
a.只含共价键
b.只含离子键
c.既含离子键,又含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物3.24 g装入元素分析装置,通入足量的氧气使之完全燃烧,将生成的气体依次通过无水CaCl2(A)管和碱石灰(B)管,测得A管增重2.16 g,B管增重9.24 g,已知该有机物的相对分子质量小于200。求该有机物的最简式和化学式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com