
| 3 |
| 2 |
| 3 |
| 2 |


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:
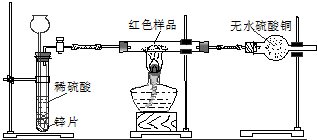
查看答案和解析>>
科目:高中化学 来源: 题型:
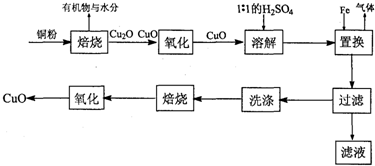
| H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | 位于元素周期表第ⅠA族,但不属于碱金属 |
| Y | 原子的最外层电子数是次外层电子数的2倍 |
| Z | 地壳中含量最多 |
| W | W+与Z2-具有相同的电子层结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
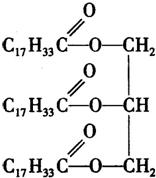 试从某油脂结构简式,分析它可能发生的化学反应:
试从某油脂结构简式,分析它可能发生的化学反应:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL 0.1mol?L-1的稀硫酸中含有SO42-个数为0.1NA |
| B、1molCH3+(碳正离子)中含有电子数为10NA |
| C、2.7g金属铝与足量的盐酸反应,铝失去电子数为3NA |
| D、12.4g白磷(分子式为P4)中含有磷原子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若将四种溶液稀释100倍,溶液pH的大小顺序:③>④>①>② |
| B、③和④分别用等浓度的硫酸溶液中和,消耗硫酸溶液的体积:③>④ |
| C、①与②混合,所得混合溶液的pH=3 |
| D、②和③混合后,溶液呈碱性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com