
分析 (1)燃烧热的热化学方程式中,可燃物必须为1mol,生成的必须是稳定的氧化物,水必须为液态,据此分析;
(2)燃烧热是在101KP时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,此时生成的水必须为液态;
(3)利用③-②可计算C(s)+H2O(g)=H2(g)+CO (g)的反应热
解答 解:(1)燃烧热是在101KP时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,故在燃烧热的热化学方程式中,可燃物必须为1mol,生成的必须是稳定的氧化物,水必须为液态,故④为燃烧热的热化学方程式,故答案为:④;
(2)燃烧热是在101KP时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,此时生成的水必须为液态,故氢气的燃烧热可以通过反应①来得到,但反应①中是2mol氢气燃烧放出570KJ的热量,故氢气的燃烧热为285KJ/mol,故答案为:285KJ/mol;
(3)将③-②可得C(s)+H2O(g)=H2(g)+CO (g)△H=(-110.5kJ/mol)-(-242kJ/mol)=+131.5kJ/mol,该反应吸热即△H>0,由于此反应中气体的种类和分子个数增多,故为熵增的反应,即△S>0,则反应若要能自发进行,应该高温下.
故答案为:C(s)+H2O(g)=H2(g)+CO (g)△H=+131.5KJ/mol;>;高温.
点评 本题考查化学反应与能量变化,为高频考点,注意把握盖斯定律的应用以及反应能否自发进行的判断,结合反应的热化学方程式解答该题,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2,2-二甲基丁烷 | B. | 2-甲基-5-乙基-1-己烷 | ||
| C. | 3-甲基-2-丁烯 | D. | 3,3-二甲基-2-戊烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
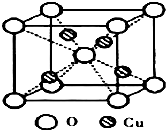 铜是过渡元素.化合物中,铜常呈现+1价或+2价.
铜是过渡元素.化合物中,铜常呈现+1价或+2价. ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
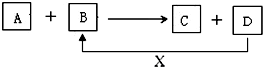 A、B、C、D、X均为中学化学常见的物质.它们之间存在如下图所示转化关系(图中反应条件略去) 填写下列空白:
A、B、C、D、X均为中学化学常见的物质.它们之间存在如下图所示转化关系(图中反应条件略去) 填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-393.5 kJ/mol | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(1)△H=-890.3 kJ/mol | |
| C. | 2H2(g)+O2(g)═2H2O(1)△H=+571.6 kJ/mol | |
| D. | $\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2(g)+3H2O(g)△H=-1400 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.44S | B. | 1S | C. | 1.33S | D. | 2S |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
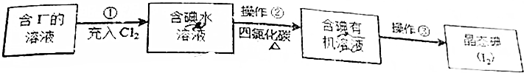
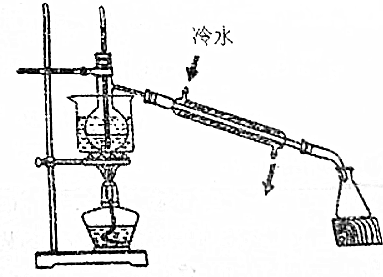
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含碳氢键数目为$\frac{a{N}_{A}}{7}$ | |
| B. | 常温常压,完全燃烧时消耗的O2一定是$\frac{33.6a}{14}$L | |
| C. | 所含共用电子对数目为($\frac{a}{7+1}$)NA | |
| D. | 所含原子总数为$\frac{a{N}_{A}}{14}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com