
 英才计划期末调研系列答案
英才计划期末调研系列答案 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
查看答案和解析>>
科目:高中化学 来源: 题型:
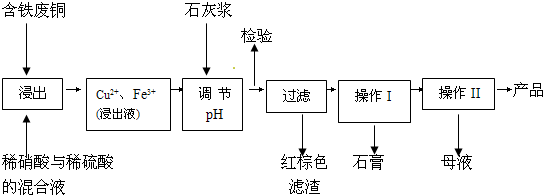
(11分)硫酸铜是一种应用极其广泛的化工原料;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2 O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:
胆矾和石膏在不同温度下的溶解度(g/100g水)见下表。
| 温度( | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红棕色滤渣的主要成分是 ;
(2)写出浸出过程中生成硫酸铜的离子方程式 ;
(3)操作I包括蒸发浓缩、 等操作,温度应该控制在  C左右;
C左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为 、 、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是 ;干燥时采用晾干,不用加热烘干的原因是 。
(5)取样检验是为了确认Fe3+是否除净。有同学设计了以下两种方案,在实验室分别对所取样品按下列方案进行操作:
方案一:取样于试管→滴加KSCN溶液; 方案二:纸层析→喷KSCN溶液;
①你认为上述两种方案设计更合理的是 ;
②指出你认为不合理方案存在的问题是 。
查看答案和解析>>
科目:高中化学 来源:2010年浙江省温州市高三上学期十校联考期中考试化学卷 题型:填空题
(11分)硫酸铜是一种应用极其广泛的化工原料;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2 O)和副产物 石膏(CaSO4·2H2O)的生产流程示意图:
石膏(CaSO4·2H2O)的生产流程示意图: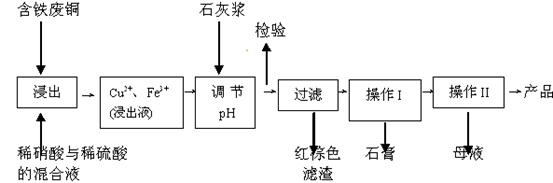
胆矾和石膏在不同温度下的溶解度(g/100g水)见下表。
温度(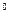 C) C) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32[来源:Z|xx|k.Com] | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8[来源:学*科*网] | 114 |
 C左右;
C左右;查看答案和解析>>
科目:高中化学 来源:2010年浙江省温州市高三上学期十校联考期中考试化学卷 题型:填空题
(11分)硫酸铜是一种应用极其广泛的化工原料;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2 O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:

胆矾和石膏在不同温度下的溶解度(g/100g水)见下表。
|
温度( |
20 |
40 |
60 |
80 |
100 |
|
石膏 |
0.32[来源:Z|xx|k.Com] |
0.26 |
0.15 |
0.11 |
0.07[来源:] |
|
胆矾 |
32 |
44.6 |
61.8 |
83.8[来源:学*科*网] |
114 |
请回答下列问题:
(1)红棕色滤渣的主要成分是 ;
(2)写出浸出过程中生成硫酸铜的离子方程式 ;
(3)操作I包括蒸发浓缩、
等操作,温度应该控制在  C左右;
C左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为 、 、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是 ;干燥时采用晾干,不用加热烘干的原因是 。
(5)取样检验是为了确认Fe3+是否除净。有同学设计了以下两种方案,在实验室分别对所取样品按下列方案进行操作:
方案一:取样于试管→滴加KSCN溶液; 方案二:纸层析→喷KSCN溶液;
①你认为上述两种方案设计更合理的是 ;
②指出你认为不合理方案存在的问题是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸铜是一种应用极其广泛的化工原料;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2 O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:
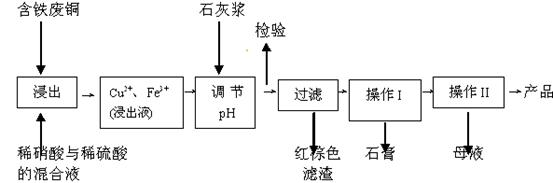
胆矾和石膏在不同温度下的溶解度(g/100g水)见下表。
| 温度( | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com