
【题目】发展“绿色食品”是提高人类生存质量的重要措施,绿色食品指( )
A.绿颜色的营养食品 B.含叶绿素的营养食品
C.植物类营养食品 D.安全无公害的营养食品
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在生物体内含量极少,但对维持生物体正常生命活动必不可少的元素有
A.Fe、Mn、Zn、Mg B.Zn、Cu、P、Ca
C.Zn、Cu、B、Mn D.K、Mn、Cu、Mo
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人对某种有机物小分子物质的样品进行分析,发现含有C、H、O、N、P等元素,这种有机小分子物质可能是
A.蛋白质 B.RNA C.麦芽糖 D.脱氧核苷酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 64 g SO2含有氧原子数为1NA
B. 物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1 NA
C. 标准状况下,22.4 L H2O的分子数为1NA
D. 常温常压下,14 g N2含有分子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将20.0g质量分数为14.0%的KNO3溶液跟30.0g质量分数为24.0%的KNO3溶液混合,得到的密度为1.15g·cm-3的混合溶液。计算:
(1)混合后溶液的质量分数___________。
(2)混合后溶液的物质的量浓度_____________。
(3)在1000g水中需溶解_____________摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________________。
(2)另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用 (选填序号)。
a.KSCN溶水 b.KSCN溶液和铁粉
c.浓氨水 d.酸性KMnO4溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应: SO2+Br2+2H2O=2HBr+H2SO4, 然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为 。
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。

(3)装置B中试剂的作用是 。
(4)认为气体Y中还含有Q的理由是 (用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于 (选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验现象应是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】R为1~18号元素,其原子所具有的电子层数为最外层电子数的![]() ,它可能形成的
,它可能形成的
含氧酸根离子有:①RO32-,②RO42-,③R2O32-,下列叙述判断正确的是
A. 当它可以形成①时,不可能形成③ B. 当它形成①时,也可以形成②和③
C. 当它可以形成②时,不可能形成③ D. 当它可以形成①时,不可能形成②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热。下图是实验室利用此反应制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)上述反应中_________是氧化剂,_________是还原剂,若反应中氧化产物比还原产物多1mol,则转移的电子数目为__________。
(2)装置B的作用是_____________,实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象:_________________。
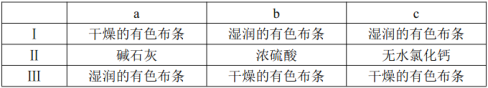
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入________(选“a”“b”或“c”)。
(4)设计装置D、E的目的是为了比较Cl2、Br2、I2的氧化性强弱。已知Br2的水溶液因浓度不同而呈现橙色或红棕色,I2难溶于水而易溶苯,且I2的苯溶液为紫红色。当向D中缓缓通入足量Cl2时,可以看到无色溶液逐渐变为红棕色,说明Cl2的氧化性大于Br2,请写出D中对应的离子方程式并用双线桥法表示出电子转移情况:________________。打开活塞,将D中的少量溶液加入E中,振荡E,观察到E中溶液分为两层,上层(苯层)为紫红色。该现象___________(填“能”或“不能”)说明Br2的氧化性大于I2。
(5)装置F的作用是除去污染性的物质(Cl2、Br2等),已知Cl2与NaOH反应时产物中可能有NaCl、NaClO、NaClO3,且c(Cl-)/c(ClO-)的值与温度高低有关。若烧杯中装有500mL0.2mol/L的NaOH溶液,则最多可吸收标况下的Cl2的体积为____________L(忽略Cl2溶于水)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com