
��֪��ӦH2��g��+ I2��g��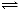 2HI��g����1 mol H2��ȫ��Ӧ�ų�a kJ�������������±����ݣ�����˵��������ǣ� ��
2HI��g����1 mol H2��ȫ��Ӧ�ų�a kJ�������������±����ݣ�����˵��������ǣ� ��
�� ѧ �� | H��H | I��I |
�Ͽ�1 mol��ѧ��ʱ���յ�������kJ�� | b | c |
A���÷�Ӧ�з�Ӧ��������������������������
B���Ͽ�1 mol H-H ����1 mol I-I �������������ڶϿ�2 mol H-I ����������
C���Ͽ�2 mol H-I����������Ϊ��a+b+c��kJ
D�����ܱ������м���2 mol H2��2 mol I2����ַ�Ӧ��ų�������С��2a kJ
 �Ͻ�ƽ���Ȿϵ�д�
�Ͻ�ƽ���Ȿϵ�д� ����ѧ��Ӧ�����ϵ�д�
����ѧ��Ӧ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�����и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ������
���ֶ�����Ԫ��A��B��C��D�����ʻ�ṹ��Ϣ���£�
��Ϣ����ԭ�Ӱ뾶��A��B��C��D ������Ԫ��֮���γɵ�ij���ַ��ӵı���ģ�ͼ������������£�
�ף� �ǵ��������������֮һ���������������������Ҫ��Դ��Լռ�������ص�����֮����
�ǵ��������������֮һ���������������������Ҫ��Դ��Լռ�������ص�����֮����
�ң� ��ɫ������ζ������ȼ���dz�����һ�ֻ�����Դ��
��ɫ������ζ������ȼ���dz�����һ�ֻ�����Դ��
���� ��ǿ�����Ե����ᣬ������������ɱ����
��ǿ�����Ե����ᣬ������������ɱ����
�����������Ϣ�ش��������⡣
��1��BԪ����Ԫ�����ڱ��е�λ��Ϊ________________����д��BC2���ӵĵ���ʽ��_______________��
��2��A���������У�EԪ�صĵ��ʻ�ԭ����ǿ��FԪ�ص�ijЩ���ೣ������ˮ����E�������Ӧ�л�����X���ɡ���д������������Ӧ�����ӷ���ʽ��
��AԪ�صĵ��������ʼ�����Ӧ��_____________________________________��
��F��C����Ԫ����ɵĻ�����Y����Ϊ���½ṹ�մɲ��ϣ�X��Y���ֻ���������Һ�з�����Ӧ��______________________________________________________��
��3�����ʶ���Ԫ����ɺͼ���ͬ�������Ӿ���18���ӽṹ����ʢ��һ��Ũ�ȶ���Һ���Թ��У���μ��������ữ������������Һ���μӹ����е�����Ϊ��
���Թ�����Һ������ػ�ɫ��������Ӧ�����ӷ���ʽΪ ��
�ڿ�ʼ���������ݳ��֣�����֤����������Ƭ�̺�Ӧ��þ��ң������μ���Һ������һ��ʱ�䣬�Թܵײ����ֺ��ɫ��������ش�Ƭ�̺�Ӧ��þ��ҡ���ԭ����a b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ��˳��Э��У��һ����ĩ��ѧ�Ծ��������棩 ���ͣ������
�״�����Ҫ�Ļ���ԭ�ϡ����úϳ���(��Ҫ�ɷ�ΪCO��CO2��H2)�ڴ����������ºϳɼ״�����������Ҫ��Ӧ���£�
��CO(g)+2H2(g) CH3OH(g) ��H1
CH3OH(g) ��H1
��CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H2=-58 kJ/mol
CH3OH(g)+H2O(g) ��H2=-58 kJ/mol
��CO2(g)+H2(g) CO(g)+H2O(g) ��H3=+41 kJ/mol
CO(g)+H2O(g) ��H3=+41 kJ/mol
�ش��������⣺
��1��CO2�ĵ���ʽ�� ��
��2����H1= kJ/mol���ٷ�Ӧ������ر��S 0(�������)��
��3�����ݻ�Ϊ2L���ܱ������У�����һ����CO2��H2�ϳɼ״�(�����ڷ�Ӧ)����������������ʱ���¶�T1��T2�Է�Ӧ��Ӱ��ͼ����ͼ������˵����ȷ����__________(�����)
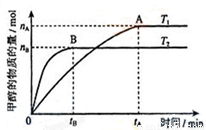
���¶�ΪT1ʱ���ӷ�Ӧ��ƽ�⣬���ɼ״���ƽ������Ϊ��v(CH3OH)=nA/tA mol/(L��min)
�ڵ�v(CH3OH) = v(H2O)ʱ��˵����Ӧ�ﵽƽ��
�ۻ�������ƽ����Է�������A�����B��
�ܴ���A��ķ�Ӧ��ϵ��T1�䵽T2���ﵽƽ��ʱn(H2)��n(CH3OH)��ֵ����
��4����T1�¶�ʱ����2molCO2��6molH2����2L�ܱ������У���ַ�Ӧ(�����ڷ�Ӧ)�ﵽƽ�����CO2ת����Ϊ50%�����������ڵ�ѹǿ����ʼѹǿ֮��Ϊ__________��T1�¶ȣ���ӦCH3OH(g)+H2O(g)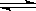 CO2(g)+3H2(g)��ƽ�ⳣ����ֵΪ__________��
CO2(g)+3H2(g)��ƽ�ⳣ����ֵΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ��˳��Э��У��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
a��b��c��d��Ϊ������Ԫ�أ�a��ԭ����ֻ��1�����ӣ�b2-��c+���ӵĵ��Ӳ�ṹ��ͬ��b��dͬ���塣����������ȷ����
A. a�ֱ���b��c��d�γɵĶ�Ԫ��������a�Ļ��ϼ۾�Ϊ+1
B. b����������Ԫ�ؾ����γ��������ֶ�Ԫ������
C. a��b�γɵĻ�������һ��ֻ�й��ۼ���b��c�γɵĻ�������һ��ֻ�����Ӽ�
D. ԭ�Ӱ뾶��С˳��d��c��b��a
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�����и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ������
A��B��C��D��E��F���ֶ���������Ԫ�أ�A�ļ�������ɫ��ӦΪ��ɫ��B������������Ӧˮ����B(OH)2 5.8 gǡ������100 mL 2 mol��L-1������ȫ��Ӧ����Bԭ�Ӻ�������������������ȡ�E2�ڻ���ɫ����C2��ȼ�ղ�����ɫ���档Dԭ�ӵ������������Ǵ�����������3����F��Dͬ���塣 �������������ش�
��1��д��Ԫ��B������ ��Ԫ��C��Ԫ�����ڱ��е�λ�� ��
��2��A��D�γɵ���ɫ������������к��еĻ�ѧ������Ϊ ��
��3��C2��ADE��Һ��Ӧ�����ӷ���ʽΪ ��
��4���õ���ʽ��ʾBC2���γɹ��� ��
��5����Ԫ��D��E���ɵ�9e���������� ��
��6���Ƚ�Ԫ��C��F����̬�⻯����ȶ��� �� ���û�ѧʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�����и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ���ǣ� ��
A��������ϩ����ϩ�������ƣ���ʹ��ˮ��ɫ
B�������Cl2�ķ�Ӧ����ϩ��Br2�ķ�Ӧ����ͬһ���͵ķ�Ӧ
C��C5H11Cl��8��ͬ���칹��
D����ͬ�����£��۷е㣺�����飼�춡��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�����и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�÷�Һ©�����Է����һ�������ǣ� ��
A���屽��ˮ B����������������
C����������Ҵ� D���Ҵ���ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ�����и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
ʵ����-25��ʱ�ɱ����壨���Ľṹ���ľ����߳�Ϊacm����Ħ������ΪMg/mol����øɱ�������ܶ�Ϊ����λ��g/cm3��
A��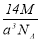 B��
B��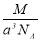 C��
C��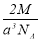 D��
D��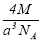
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���½��������������и߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
Ԫ��X��Y��Z�����ڱ��е����λ����ͼ��ʾ����֪YԪ��ԭ�ӵ���Χ�����Ų�Ϊns��n��1��np��n��1����������˵������ȷ���ǣ� ��
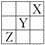
A. YԪ��ԭ�ӵ���Χ�����Ų�Ϊ4s24p4
B. YԪ�������ڱ��ĵ������ڢ�A��
C. XԪ�����������������ǽ���Ԫ�����
D. ZԪ��ԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s23p63d104s24p3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com