
用铁酸钠(Na2FeO4)对河湖的淡水消毒是城市饮用水处理新技术,下列对Na2FeO4用于饮用水消毒处理的分析正确的是( )
A.Na2FeO4在溶液中显强酸性,能消毒杀菌
B.在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌
C.Na2FeO4的还原产物Fe3+易水解为Fe(OH)3胶体,可使水中悬浮物凝聚沉降 D.Na2FeO4的还原产物Fe2+易水解为Fe(OH)2胶体,可使水中悬浮物凝 聚沉降
聚沉降
科目:高中化学 来源: 题型:
据《自然》杂志报道,在300~400℃的高温下,将砂糖(主要成分为蔗糖)等碳水化合物用加热的方法使其形成焦糖与碳之间的“半成品碳”状态,再放进硫酸溶液中高温加热,生成了一种叫“焦糖烯”的物质,其分子式为C36H50O25。下列有关说法正确的是
A.“半成品碳”在硫酸溶液中加热可能发生的是消去反应
B.“半成品碳”是碳元素的一种新单质
C. 蔗糖溶液与新制的氢氧化铜悬浊液混合加热有砖红色沉淀生成
D. 焦糖烯是一种新型的烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,NO2跟NH3可以发生反应生成N2和H2O,反应方程式为6NO2+8NH3=7N2+12H2O。请回答:
(1)标明电子转移的方向和数目;
(2)氧化产物与还原产物的质量比是 ;
(3)若经氧化得到的N2比经还原得到的N2多2.8g,求参加反应的NO2 和NH3的质量各是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
镭是元素周期表中第ⅡA族元素,下列关于镭的叙述不正确的是( )
A. 镭比钙的金属性更强 B. 在化合物中是+2价
C. 镭是一种放射性元素 D. 氢氧化镭呈两性
查看答案和解析>>
科目:高中化学 来源: 题型:
氮氧化铝(AlON)是一种透明高硬度防弹材料,可以由反应Al2O3+C+N2=2AlON+CO(高温)合成,下列有关说法正确的是
A.氮氧化铝中氮的化合价是-3
B.反应中氮气作氧化剂
C.反应中每生成5.7g AlON 同时生成1.12 L CO
D.反应中氧化产物和还原产物的物质的量之比是2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
C、O、Na、Al、S、Cl是常见的六种元素
(1)C元素位于元素周期表第 周期,第 族;C元素的一种同位素可以测定文物年代,这种同位素的符号为
(2)用“大于”“小于”或“等于”填空
| 离子半径 | 酸性 | 还原性 | 得电子能力 |
| N3- Al3+ | H2SO4 HClO4 | O2- S2- | 35Cl 37Cl |
(3)① CaCO3和适量HCl溶液反应时,每产生4.4 g 气体(不考虑气体溶解),放热a kJ,则该反应的热化学方程式为 。
②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得pH变化曲线如图所示

请用离子方程式表示B-C段发生的反应:
(4)氢气、氧气常用来作燃料电池,写出电解质为氢氧化钠溶液时
负极上的电极方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
在一容积可变的密闭容器中,aA(气)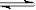 bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
A.平衡向正反应方向移动了 B.物质A的转化率减少了
C.物质B的质量分数减小了 D.化学计量数关系a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题
(1)根据计算用托盘天平需称取氯化钠 g。
(2)配制时,必须用到的玻璃仪器有烧杯 玻璃棒 与
(3)配制溶液有下列几步操作:a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,
f.将溶液移至容量瓶,g.贴标签,h.定容。
则正确的操作顺序是 。
(4)下列操作结果使溶液物质的量浓度偏低的是
A.没有将洗涤液转入容量瓶中, B.容量瓶洗涤后,未经干燥处理,
C.定容时,俯视容量瓶的刻度线, D.加水定容时,水的量超过了刻度线。
(5)取出该NaCl溶液10mL加水稀释到100mL,稀释后溶液中NaCl的
物质的量浓度是 。
(6)写出检验NaCl溶液中含有氯离子的有关反应方程式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com