
阿斯巴甜是目前使用最广泛的甜味剂.甜度约为蔗糖的200倍,其结构简式为:

下列关于阿斯巴甜的说法正确的是( )
A.分子式为C14H19N2O5 B.既能与酸反应又能与碱反应
C.不能发生水解反应 D.1mol该物质最多可与2molNaOH反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年云南省高一上期中化学试卷(解析版) 题型:选择题
下列实验问题的处理方法中,正确的是( )
A. 实验中不慎打破温度计,可用吹风机加快水银的蒸发
B. 在气体发生装置上直接点燃甲烷气体时,必须先检验甲烷的纯度
C. 实验结束后,将废液倒入下水道排出实验室,以免污染实验室
D. 燃着的酒精灯不慎碰翻失火,应立即用水扑灭
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海师大附中高二上期中化学试卷(解析版) 题型:选择题
某学生用碱式滴定管量取NaOH溶液,开始时仰视液面,读数为5.00 mL,取出部分溶液后,俯视液面,读数为15.00 mL,该同学在操作中实际取出的液体为
A.大于10.00 mL B.小于10.00 mL C.等于10.00 mL D.等于11.00 mL
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上期中化学卷(解析版) 题型:推断题
软质隐形眼镜材料W、树脂X的合成路线如图所示。

(1)A中含有的官能团的结构简式是_______________。
(2)甲的结构简式是_______________。
(3)B→C反应的化学方程式是____________________________。
(4)B有多种同分异构体.属于酯且含有碳碳双键的同分异构体共有______________种(不考虑顺反异构。
(5)已知F的相对分子质量为110,1molF可与足量钠反应生成22.4L氢气(标准状况下),
苯环上的氢原子化学环境都相同.则F还能发生的反应是 _______________(填序号)
_______________(填序号)
a.加成反应 b.氧化反应 c.加聚反应 d.水解反应
(6)写出树脂X可能的结构简式_______________(写出一种即可)。
(7)E的分子式为C10H14O2,含三个甲基,苯环上的一溴代物有两种,生成E的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上期中化学卷(解析版) 题型:选择题
已知苯环上由于取代基的影响,使硝基邻位上的卤原子的反应活性增强,现有某有机物的结构简式如下:
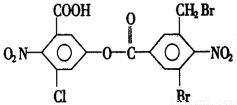
1mol该有机物与足量的氢氧化钠溶液混合并共热,充分反应后最多可消耗氢氧化钠的物质的量为a(不考虑醇羟基和硝基与氢氧化钠的反应,下同),溶液蒸干得到的固体产物再与足量的干燥碱石灰共热,又消耗氢氧化钠的物质的量为b,则a,b分别是( )
已知: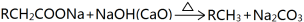
A.5mol,10mol B.6mol,2mol C.8mol,4mol D.8mol,2mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上期中化学卷(解析版) 题型:选择题
下列几种有机物:(a)饱和一元醇,(b)饱和一元醛,(c)饱和一元羧酸,(d)饱和一元醇和饱和一元羧酸生成的酯,(e)乙炔的同系物,(f)苯的同系物,其中完全燃烧产生的水和二氧化碳的物质的量之比是恒定的有( )
A.(b)(c)(d) B.(a)(d) C.(b)(c)(d)(e)(f) D.(b)(c)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上期中化学卷(解析版) 题型:实验题
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(2)要加快上述实验中气体产生的速率,还可采取的措施有: 、 (答两种);
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
实验 混合溶液 | A | B | C | D | E | F |
4mol/L H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
① 完成此实验设计,其中:V1= ,V6= ,V9= ;
完成此实验设计,其中:V1= ,V6= ,V9= ;
②同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因  。
。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上月考二化学卷(解析版) 题型:填空题
电化学综合应用
(Ⅰ) 选择合适的图象:
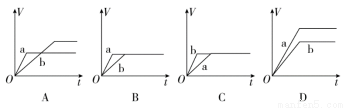
(1)将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是_____________。
(2)将(1)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图象是 。
(Ⅱ)如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
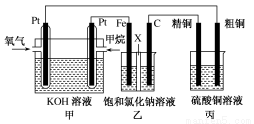
(1)甲烷燃料电池负极反应式是_________________________。
(2)乙装置中铁极的电极反应式为_______________________。
(3)检验石墨(C)极反应产物的方法是____________ _________。
(4)若在标准状况下,有2.24 L氧气参加反应,丙装置中阴极析出铜的质量为________g。
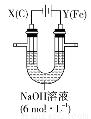
(Ⅲ)Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的高效水处理剂,其电解制法如图所示。电解过程中,两极均有气体产生,Y极区域溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍澄清。查阅资料得知,高铁酸根离子(FeO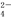 )在溶液中呈紫红色。
)在溶液中呈紫红色。
(1)电解过程中,X极区溶液的pH___________(填“增大”“减小”或“不变”)。
(2)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-===FeO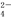 +4H2O和_____ _____。
+4H2O和_____ _____。
(3)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少__________g。
(4)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn===Fe2O3+ZnO+2K2ZnO2。该电池正极发生的反应的电极反应式为____________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学卷(解析版) 题型:选择题
下列表述中正确的是
A.任何能使熵值增大的过程都自发进行
B.已知热化学方程式2SO2(g)+O2(g) 2SO3(g) ΔH=-Q kJ·mol-1(Q>0),则将2mol SO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量
2SO3(g) ΔH=-Q kJ·mol-1(Q>0),则将2mol SO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量
C.人类利用的能源都是通过化学反应获得的
D.1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者放出的热量多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com