解:(Ⅰ)(1)配制的是220mL溶液,实验室中没有220mL容量瓶,需要选用250mL容量瓶,
故答案是:250;
(2)配制的溶液含有的硫酸的物质的量是:0.25×1=0.25mol,需要质量分数为98%的浓硫酸(密度为1.84g/cm
3)的体积是:

L≈0.0136L=13.6mL,需要使用25mL量筒量取,
故答案是:13.6;C;
(3)配制步骤是:计算、量取浓硫酸、浓硫酸的稀释、转移、洗涤、定容,即③①④②,
故答案是:③①④②;
(4)检查容量瓶是否漏水的方法是:用右手食指顶住瓶塞,用左手拖住瓶底,将容量瓶倒转过来看瓶口处是否有水渗出,若没有,将瓶塞旋转180度,重复上述操作,如果瓶口处仍无水渗出,则容量瓶不漏水,
故答案是:用右手食指顶住瓶塞,用左手拖住瓶底,将容量瓶倒转过来看瓶口处是否有水渗出,若没有,将瓶塞旋转180度,重复上述操作,如果瓶口处仍无水渗出,则容量瓶不漏水;
(5)由于刚刚洗涤洁净的量筒内壁有有蒸馏水,量取的浓硫酸体积偏小,配制的溶液浓度偏低,
故答案是:偏低;
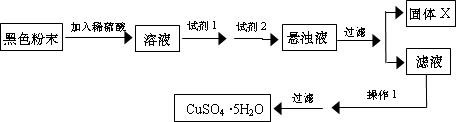
(Ⅱ)①不能用量筒溶解氢氧化钠,应该使用烧杯,操作错误,故①正确;
②用玻璃棒搅拌加速溶解,操作正确,故②错误;
③转移溶液到容量瓶中后,适当晃动容量瓶的操作,操作正确,故③错误;
④转移溶液必须用玻璃棒引流,操作错误,故④正确;
⑤眼睛与刻度线相平,图中操作错误,故⑤正确;
⑥最后摇匀容量瓶内的溶液操作,操作正确,故⑥错误;
符合题意的有:①④⑤
故答案是:①④⑤.
分析:(Ⅰ)(1)配制220mL稀硫酸,需要250mL容量瓶;
(2)配制1mol/L的稀硫酸250mL,算出硫酸的物质的量,再计算出需要浓硫酸溶液的体积;根据计算结果选择量筒;
(3)根据配制一定物质的量浓度的溶液配制步骤排序;
(4)根据检查容量瓶是否漏水的操作方法完成;
(5)量筒内壁有水,导致量取的浓硫酸体积偏小;
(Ⅱ)根据配制一定物质的量浓度的溶液的正确操作方法进行判断.
点评:本题考查了配制一定物质的量浓度的溶液的配制方法,注重了基础知识的基础,题量较多,难度不大.

 L≈0.0136L=13.6mL,需要使用25mL量筒量取,
L≈0.0136L=13.6mL,需要使用25mL量筒量取,