
| 选项 | 现象或事实 | 解释 |
| A | 常温下将Al片放入浓硝酸中无明显变化 | Al与浓硝酸不反应 |
| B | 加热滴有酚酞的醋酸钠溶液,溶液红色变深 | 加热促进CH3COO-水解,溶液的碱性增强 |
| C | 将溴水分别滴入植物油和裂化汽油中,溴水均褪色 | 前者由于萃取而褪色,后者由于发生加成反应而褪色 |
| D | 加热NaHCO3溶液无明显变化 | NaHCO3的热稳定性强 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.常温下将Al片放入浓硝酸中发生钝化;
B.醋酸钠溶液中醋酸根离子水解显碱性,水解是吸热过程,加热促进水解;
C.植物油和裂化汽油中均含碳碳双键;
D.加热NaHCO3溶液无明显变化,但加热NaHCO3固体则发生分解生成碳酸钠、水和二氧化碳.
解答 解:A.常温下将Al片放入浓硝酸中发生钝化,生成致密的氧化膜阻止反应的进一步发生,则观察不到明显现象,并不是不反应,故A错误;
B.醋酸钠溶液中醋酸根离子水解显碱性,水解是吸热过程,加热促进水解碱性增强,所以加热滴有酚酞的醋酸钠溶液,碱性增强,溶液红色变深,故B正确;
C.植物油和裂化汽油中均含碳碳双键,均与溴水发生加成反应,故C错误;
D.加热NaHCO3溶液无明显变化,但加热NaHCO3固体则发生分解生成碳酸钠、水和二氧化碳,所以NaHCO3受热易分解,稳定性弱,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及Al的钝化、盐类水解及植物油和裂化汽油的结构等,把握物质的性质及发生的化学反应、反应原理为解答的关键,注意实验的评价性分析,题目难度不大.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:多选题
| A. | C2H4和C2H20一定互为同系物 | |
| B. | 丙氨酸和苯丙氨酸脱水缩合,最多可生成3种二肽 | |
| C. | 葡萄糖在人体内被氧化,最终转化为二氧化碳和水,并释放能量 | |
| D. | 向鸡蛋清溶液中加入饱和(NH4)2SO4溶液,有沉淀析出,再加水沉淀会溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
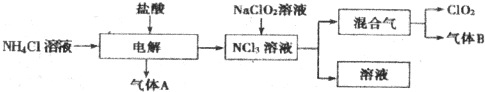
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
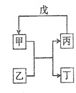 甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( )
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化).下列各组物质中,不满足图示转化关系的是( )| 选项 | 甲 | 乙 | 丙 | 戊 |
| A | NH3 | O2 | NO | H2O |
| B | Fe | H2O | H2 | Fe2O3 |
| C | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | 过量CO2 |
| D | Na2O2 | CO2 | O2 | Na |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- | |
| B. | 溶液中含大量Al3+:HClO、HCO3-、ClO-、CO32- | |
| C. | 能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- | |
| D. | 中性的溶液中:CO32-、Na+、SO42-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 | |
| B. | 高锰酸钾溶液和双氧水的消毒原理相同 | |
| C. | 双氧水具有较强的腐蚀性,不能用于清洗创口 | |
| D. | 在次氯酸钠溶液中通入少量二氧化硫可得到亚硫酸钠和次氯酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
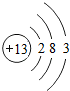 ,Al(OH)3的碱性比Mg(OH)2弱(填“强”或“弱”).
,Al(OH)3的碱性比Mg(OH)2弱(填“强”或“弱”). .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素、蛋白质都是天然有机高分子化合物 | |
| B. | 食用植物油的重要成分是高级不饱和脂肪酸甘油酯,不是天然高分子化合物 | |
| C. | 禁止使用含铅汽油是为了提高汽油的燃烧效率 | |
| D. | 碱液去污属于化学变化,洗涤剂去污主要是物理变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com