
【题目】关于NA下列说法正确的是
A. 常温常压下,17g羟基(—18OH)所含中子数为9NA
B. 0.1mol NH3溶于水形成的溶液中,微粒NH3·H2O和微粒NH4+的数目之和为0.1NA
C. 常温下电解饱和食盐水,当溶液pH值由7变为12时,电路中转移的电子数为0.01NA
D. 标准状况下,足量的甲烷与22.4LCl2(假设氯气完全反应)在光照条件下发生取代反应,形成C-Cl键的数目为NA
【答案】D
【解析】
A. 17g羟基(—18OH)的物质的量=![]() =
=![]() mol,一个-18OH含有10个中子,所含中子为
mol,一个-18OH含有10个中子,所含中子为![]() ×10 mol=
×10 mol=![]() mol,故A错误;
mol,故A错误;
B. NH3溶于水,发生NH3 + H2O ![]() NH3·H2O
NH3·H2O![]() NH4++OH-,根据物料守恒,0.1mol NH3溶于水形成的溶液中存在NH3、NH3·H2O、NH4+,微粒NH3·H2O和微粒NH4+的数目之和小于0.1NA,故B错误;
NH4++OH-,根据物料守恒,0.1mol NH3溶于水形成的溶液中存在NH3、NH3·H2O、NH4+,微粒NH3·H2O和微粒NH4+的数目之和小于0.1NA,故B错误;
C. 溶液体积不明确,故溶液中放电的氢离子的物质的量无法计算,则转移的电子数无法计算,故C错误;
D. 标准状况下,22.4LCl2的物质的量为1mol,足量的甲烷与1molCl2(假设氯气完全反应)在光照条件下发生取代反应,每取代一个H,就会形成一个C—Cl键和一个H—Cl键,故该反应生成4种取代产物(共1mol)和1molHCl,形成1molC-Cl键,数目为NA,故D正确;
答案选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,其熔点64.5℃,沸点5.5℃,遇水易水解。它是有机合成中的重要试剂,可由NO与Cl2在常温常压下合成。
(1)实验室制备原料气NO和Cl2的装置如下图所示:
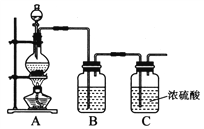
实验室制Cl2时,装置A中烧瓶内发生反应的化学方程式为_______。装置B中盛放的试剂为_______,其作用为___________________。
(2)将上述收集到的Cl2充入D的集气瓶中,按图示装置制备亚硝酰氯。

①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_______。
②装置D中发生的反应方程式为__________________。
③如果不用装置E会引起什么后果______________________。
④某同学认为装置F不能有效吸收尾气中的某种气体,该气体为_____,为了充分吸收尾气,可将尾气与_______同时通入氢氧化钠溶液中。
(3)工业上可用间接电化学法除去NO,其原理如下图所示,吸收塔中发生的反应为:NO+S2O42+H2O→N2+HSO3

①吸收塔内发生反应的氧化剂与还原剂物质的量之比为_________________。
②阴极的电极反应式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食醋是常用的食品酸味剂,其主要成分是乙酸。下列有关乙酸说法不正确的是( )
A.乙酸易溶于水
B.食醋可由粮食酿造
C.乙酸可与苏打反应
D.乙酸不易挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,将1.0L w molL-1CH3COOH溶液与0.1molNaOH固体混合,充分反应。然后向混合液中加入CH3COOH或 CH3COONa固体(忽略溶液体积和温度变化),溶液pH变化如图所示。下列叙述正确的是

A. a、b、c对应的溶液中,水的电离程度由大到小的顺序是:c>a>b
B. w≥0.1
C. 从b到a的过程中,[c(Na+)·c(OH-)]/c(CH3COO-)增大
D. 25℃时,CH3COOH的电离平衡常数![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐和CO2、H2O。某同学利用下述系列反应实现了“铜![]() 铜绿
铜绿![]() ……
……![]() 铜”的转化。
铜”的转化。
铜![]() 铜绿
铜绿![]() A
A![]() Cu(OH)2
Cu(OH)2![]() B
B![]() Cu
Cu
(1)从三种不同分类标准回答,“铜绿”属于哪类物质?____。
(2)写出B的化学式____。
(3)上述转化过程中属于置换反应的是____(填序号)。
(4)写出①反应的化学方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作完全正确的个数是是( )
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛装液体体积超过试管容积三分之一的试管加热 ③鼻子靠近容器口去闻气体的气味 ④将试管平放,用纸槽将固体粉末送入试管底部,然后竖立试管⑤蒸馏实验时温度计应伸入液面以下测量液体温度 ⑥将烧瓶放在桌上,用力塞紧瓶塞 ⑦用坩埚钳夹取加热后的蒸发皿 ⑧蒸馏实验加热时发现蒸馏烧瓶中未加沸石则应迅速补加防止暴沸 ⑨稀释浓硫酸时,把水倒入盛有浓硫酸的量筒中 ⑩蒸馏实验先点燃酒精灯后再通冷凝水
A.3个B.4个C.5个D.6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用中和滴定法测定某烧碱的纯度,试根据实验回答:
(1)称取4.1g烧碱样品。将样品配成250mL待测液,需要的主要玻璃仪器除烧杯、玻璃棒外还需__________________ 、______________________。
(2)取10.00mL待测液,用___________________量取。
(3)用0.2010mol·L-1标准盐酸滴定待测烧碱溶液,以酚酞为指示剂,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视_____________,直到看到______________________________即可判断达到滴定终点。
(4)根据下列数据,计算待测烧碱溶液的浓度为:_____________________(结果保留四位有效数字),样品烧碱的质量分数为________________(结果保留四位有效数字)。(假设烧碱中不含有与酸反应的杂质)
滴定次数 | 待测液体积 (mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 10.00 | 0.50 | 20.40 |
第二次 | 10.00 | 4.00 | 24.10 |
(5)滴定过程,下列情况会使测定结果偏高的是_____________________________填序号)。
①酸式滴定管用水洗后便装液体进行滴定;②碱式滴定管水洗后,就用来量取待测液;③锥形瓶用蒸馏水洗涤后,又用待测液润洗;④滴定过快成细流、将碱液溅到锥形瓶壁而又未摇匀洗下;⑤盐酸在滴定时溅出锥形瓶外;⑥滴加盐酸,溶液颜色褪去但不足半分钟又恢复红色;⑦滴定前,酸式滴定管有气泡,滴定后消失;⑧记录起始体积时,仰视读数,终点时俯视。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ\(1)“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化剂及军事科学中。所谓“纳米材料”是指研究、开发出的微粒直径从几纳米到几十纳米的材料,如将纳米材料分散到分散剂中,所得混合物可能具有的性质是 ____。
A.能全部透过滤纸 B.有丁达尔效应 C.所得液体呈胶状 D.所得物质一定是悬浊液
(2)把淀粉溶液溶于沸水中,制成淀粉胶体,鉴别溶液和淀粉胶体可以利用的方法是__________。
(3)把少量的FeCl3饱和溶液滴入沸水中,制成Fe(OH)3胶体后滴入少量稀硫酸可观察到的现象是:__,继续滴加至稀硫酸过量可观察到的现象是_____,写出上述反应的化学方程式____。
Ⅱ\给下图①~⑤选择适当的物质,使有连线的两物质能发生反应。供选择的试剂有稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉。

(1)请推断它们的化学式分别为:②______,③ ______,⑤_______。
(2)写出下列序号之间的化学方程式:①和②:_______________,②和④:____________,③和④:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学反应与能量的说法正确的是
A. 中和反应是吸热反应B. 燃烧属于放热反应
C. 化学键断裂放出能量D. 反应物总能量与生成物总能量一定相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com