
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 用小苏打治疗胃酸过多:HCO${\;}_{3}^{-}$+H+═H2O+CO2↑ | |
| C. | 石灰石与盐酸反应:CO32-+2 H+═H2O+CO2↑ | |
| D. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
分析 A.电子不守恒;
B.反应生成氯化钠、水、二氧化碳;
C.碳酸钙在离子反应中保留化学式;
D.电子、电荷不守恒.
解答 解:A.钠与水反应的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.用小苏打治疗胃酸过多的离子反应为HCO3-+H+═H2O+CO2↑,故B正确;
C.石灰石与盐酸反应的离子反应为CaCO3+2H+═H2O+CO2↑+Ca2+,故C错误;
D.铜片插入硝酸银溶液中的离子反应为Cu+2Ag+═Cu2++2Ag,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.


科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 消耗128g S时,反应转移的电子总物质的量为164mol | |
| B. | 消耗12gC时,反应转移4mol电子 | |
| C. | 被氧化和被还原的硫原子之比为3:1 | |
| D. | KNO3发生了氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 (R、R′代表烃基)
(R、R′代表烃基)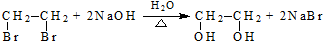 .
. .
.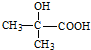 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com