
������ͼ��ʾһ����̼��ԭ�����������ʵ��װ�ã��ش��������⡣
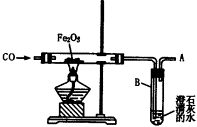
��1���ж�Ӳ�ʲ��������ѿ�ʼ������Ӧ�ķ�����________��
��2����Ӧ�����з�����������________��
��3����A����ȼ�ɼ�dz��ɫ�����ԭ����________��
��4��ʵ�����ʱӦע��IJ�����________������ţ���
����ֹͣͨ��CO������Ϩ��ƾ��ƣ�������ͨ��CO����Ϩ��ƾ��ƣ�ͬʱֹͣͨ��CO������Ϩ��ƾ��ƣ�����ͨ��CO������ȼ�ų���CO���塣
��5������0.1g����ij�������������CO��ȫ��ԭ����B�п��˵�0.1724g�������ʣ���֪ʯ��ˮ����������ȷ������������Ļ�ѧʽ��
 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
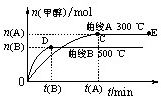 9��һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO��g��+2H2��g��
9��һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO��g��+2H2��g�� CH3OH��g��
CH3OH��g�� 2Cu+CO2
2Cu+CO2 2Cu+CO2
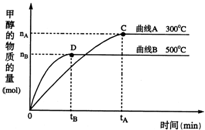
2Cu+CO2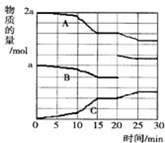 ��4����Ӧ������CO��g����H2��g����CH3OH��g�����ʵ����仯��ͼ��ʾ���ֱ���A��B��C��ʾCO��H2��CH3OH������ͼ����ʾ�ж�����˵����ȷ����
��4����Ӧ������CO��g����H2��g����CH3OH��g�����ʵ����仯��ͼ��ʾ���ֱ���A��B��C��ʾCO��H2��CH3OH������ͼ����ʾ�ж�����˵����ȷ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| �ŵ� | ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ý�̿����Ȼ����ȡ���۵�CO��H2�������ڰ��ϳɺ��л��ϳ���Ŀǰ��ҵ��������Ҫ;����
���ý�̿����Ȼ����ȡ���۵�CO��H2�������ڰ��ϳɺ��л��ϳ���Ŀǰ��ҵ��������Ҫ;����
| ||
| c(CH3OH) |
| c(CO)?c2(H2) |
| c(CH3OH) |
| c(CO)?c2(H2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������������ ���ͣ�022
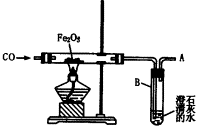
��1���ж�Ӳ�ʲ��������ѿ�ʼ������Ӧ�ķ�����________��
��2����Ӧ�����з�����������________��
��3����A����ȼ�ɼ�dz��ɫ�����ԭ����________��
��4��ʵ�����ʱӦע��IJ�����________������ţ���
����ֹͣͨ��CO������Ϩ��ƾ��ƣ�������ͨ��CO����Ϩ��ƾ��ƣ�ͬʱֹͣͨ��CO������Ϩ��ƾ��ƣ�����ͨ��CO������ȼ�ų���CO���塣
��5������0.1g����ij�������������CO��ȫ��ԭ����B�п��˵�0.1724g�������ʣ���֪ʯ��ˮ����������ȷ������������Ļ�ѧʽ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com