
【题目】酯类化合物H是一种医药中间体,常用于防晒霜中紫外线的吸收剂。实验室由化合物A和E制备H的一种合成路线如下图:

已知
①![]()
②![]()
回答下列问题:
(1)经测定E的相对分子质量为28,常用来测定有机物相对分子质量的仪器为___________。
F中只有一种化学环境的氢原子,其结构简式为_________________。
G中只有一种官能团,F→G的反应类型为___________________。
(2)(CH3)2SO4是一种酯,其名称为_________________。
(3)A能与Na2CO3溶液及浓溴水反应,且1molA最多可与2molBr2反应。核磁共振氢谱表明A的苯环上有四种不同化学环境的氢原子。A的结构简式为________________。C中含氧官能团的结构简式为_________。
(4)D+G→H的化学方程式为__________________。
(5)C的同分异构体中能同时满足下列条件的共有_____种(不含立体异构)。
①遇FeCl3溶液发生显色反应 ②能发生水解反应
(6)参照上述合成路线,设计一条由![]() 和(CH3)3CCl为起始原料制备
和(CH3)3CCl为起始原料制备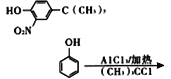 的合成路线(其他试剂任选);____________________
的合成路线(其他试剂任选);____________________
【答案】 质谱仪 ![]() (或
(或![]() ) 水解反应或加成反应 硫酸二甲酯
) 水解反应或加成反应 硫酸二甲酯 ![]() -COOH、
-COOH、![]()
 19
19 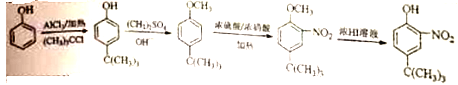
【解析】(1)常用来测定有机物相对分子质量的仪器为质谱仪;经测定E的相对分子质量为28,应该为乙烯,乙烯氧化生成F,F中只有一种化学环境的氢原子,分子式为C2H4O,则F应该为环氧乙烷,其结构简式为![]() 或
或![]() ;F与水反应生成G, G中只有一种官能团,根据G的分子式可知G为乙二醇,故F→G的反应类型为加成反应或水解反应;(2)(CH3)2SO4是一种酯,由甲醇与硫酸发生酯化反应而得,其名称为硫酸二甲酯;(3)A能与Na2CO3溶液及浓溴水反应,则为酚,根据反应原理和B的分子式可推知A为甲基苯酚,酚羟基的邻、对位上的氢能被溴取代,1molA最多可与2molBr2反应,说明甲基在邻位或对位上;核磁共振氢谱表明A的苯环上有四种不同化学环境的氢原子,则甲基在邻位(若在对位则苯环上只有两种不同环境下的氢),故A的结构简式为
;F与水反应生成G, G中只有一种官能团,根据G的分子式可知G为乙二醇,故F→G的反应类型为加成反应或水解反应;(2)(CH3)2SO4是一种酯,由甲醇与硫酸发生酯化反应而得,其名称为硫酸二甲酯;(3)A能与Na2CO3溶液及浓溴水反应,则为酚,根据反应原理和B的分子式可推知A为甲基苯酚,酚羟基的邻、对位上的氢能被溴取代,1molA最多可与2molBr2反应,说明甲基在邻位或对位上;核磁共振氢谱表明A的苯环上有四种不同化学环境的氢原子,则甲基在邻位(若在对位则苯环上只有两种不同环境下的氢),故A的结构简式为![]() ;
;![]() 在碱性条件下与(CH3)2SO4反应生成B,B为
在碱性条件下与(CH3)2SO4反应生成B,B为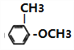 ;
; 被酸性高锰酸钾氧化生成C,C为
被酸性高锰酸钾氧化生成C,C为![]() ,含氧官能团的结构简式为-COOH、
,含氧官能团的结构简式为-COOH、![]() ;(4)C在浓氢碘酸中反应生成D,D为
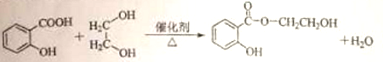
;(4)C在浓氢碘酸中反应生成D,D为![]() ;D+G→H为
;D+G→H为![]() 与HOCH2CH2OH在催化剂及加热条件下反应生成H和水,H为
与HOCH2CH2OH在催化剂及加热条件下反应生成H和水,H为![]() ,反应的化学方程式为
,反应的化学方程式为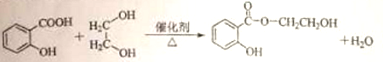 ;(5)
;(5)![]() 的同分异构体满足:①遇FeCl3溶液发生显色反应,则含有酚羟基;②能发生水解反应则含有酯基。结构C的结构简式可推知,若苯环上有两个取代基,则取代基可以是酚羟基和HCOOCH2-或CH3COO-或CH3OOC-,而位置上有邻、间、对位,则结构有3
的同分异构体满足:①遇FeCl3溶液发生显色反应,则含有酚羟基;②能发生水解反应则含有酯基。结构C的结构简式可推知,若苯环上有两个取代基,则取代基可以是酚羟基和HCOOCH2-或CH3COO-或CH3OOC-,而位置上有邻、间、对位,则结构有3![]() 3=9种;若取代基为三个,则为
3=9种;若取代基为三个,则为
CH3-、HCOO-、酚羟基,先定两个取代基,再定第三个取代基,则若甲基和酚羟基在邻位时HCOO-取代有四种,若甲基和酚羟基在间位时HCOO-取代有四种,若甲基和酚羟基在对位时HCOO-取代有两种共10种,故总计符合条件的有19种同分异构体;(6)根据②![]() 由
由![]() 和(CH3)3CCl在氯化铝催化下反应生成
和(CH3)3CCl在氯化铝催化下反应生成![]() ,
,![]() 在碱性条件下与(CH3)2SO4反应生成
在碱性条件下与(CH3)2SO4反应生成![]() ,
,![]() 在浓硫酸催化下与浓硝酸发生硝化反应生成
在浓硫酸催化下与浓硝酸发生硝化反应生成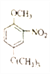 ,
, 在浓氢碘酸中反应生成D,
在浓氢碘酸中反应生成D,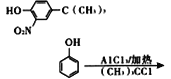 ,合成路线为:
,合成路线为: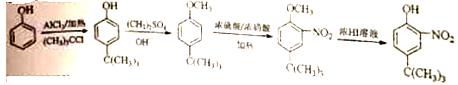 。
。


科目:高中化学 来源: 题型:
【题目】某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) ![]() 2Z(g)+W(s)-Q(Q>0),下列叙述中,正确的是
2Z(g)+W(s)-Q(Q>0),下列叙述中,正确的是
A. 反应过程中,气体的密度始终不变
B. 当容器中气体压强不变时,反应达到平衡状态
C. 当2v正(X)=v逆(Z)时,反应达平衡状态
D. 升高温度,v(正)增大、v(逆)减小,平衡向正反应移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香酯I的合成路线如下:

已知以下信息:
①A~I均为芳香族化合物,B苯环上只有一个取代基,且B能发生银镜反应;D的相对分子质量比C大4,E的核磁共振氢谱有3组峰。
②![]() ③
③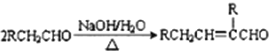
请回答下列问题:
(1)A→B的反应类型为____________,G中所含官能团的名称有____________________,E的名称是______________________________。
(2)B与银氨溶液反应的化学方程式为______________________________。
(3)I的结构简式为______________________________。
(4)符合下列要求A的同分异构体还有_______________种。
①与Na反应并产生H2 ②芳香族化合物
(5)据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2CH2OH的合成路线流程图(无机试剂任选)。合成路线流程图示如下:CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3。
CH3COOCH2CH3。
_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验现象及其解释不正确的是
A. 金属钠在Cl2中燃烧产生白烟,这是因为产生的NaCl固体颗粒分散到空气中所致
B. 把烧红的铁丝放在氧气中,发出耀眼白光,产生黑色固体,这是因为该反应放热多,生成的Fe3O4为黑色
C. 单质Mg、Al与O2反应,条件不同,可能产生不同的产物
D. 镁带在空气中点燃发出耀眼光芒,并发生三个反应:2Mg+O2![]() 2MgO、3Mg+N2
2MgO、3Mg+N2![]() Mg3N2、2Mg+CO2
Mg3N2、2Mg+CO2![]() 2MgO+C(黑色),Mg常用于照明弹。在这些反应中,Mg都是作还原剂
2MgO+C(黑色),Mg常用于照明弹。在这些反应中,Mg都是作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用离子方程式解释下列问题
(1)A12S3为什么不能用Na2S溶液和A1C13溶液制备_____________________________________。
(2)泡沫灭火器原理_____________________________________。
(3)氯化铁溶液蒸干并灼烧的产物是________________________,原因是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的理解不正确的是( )
A.摩尔是一个物理量
B.摩尔是物质的量的单位,简称摩,符号为mol
C.1mol12C与0.012kg12C所含碳原子数相同
D.1molO2约含6.02×1023个氧分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛(HCHO)与葡萄糖相似具有强还原性,40%甲醛溶液沸点为96℃,易挥发。为探究过量甲醛和新制Cu(OH)2反应的产物,进行如下研究。
(1)在如图装置中进行实验,向a中加入0.5 mol/LCuSO4溶液50 mL和5 mol/LNaOH溶液100 mL,振荡,再加入40%的甲醛溶液50 mL,缓慢加热a,在65 ℃时回流20分钟后冷却至室温。反应过程中观察到有棕色固体生成,最后变成红褐色,并有气体产生。

①仪器b的名称是_________,作用为_________。
②能说明甲醛具有还原性的实验现象是______________。
(2)查阅资料发现气体产物是副反应产生的。为确认气体产物含H2不含CO,将装置A和如图所示的装置连接后进行实验。
依次连接的合理顺序为A→B→___→_____→_____→_____→G,__________装置B的作用是______。
(3)已知:![]() 。设计实验证明a中甲醛的碳元素未被氧化成+4 价,___________。
。设计实验证明a中甲醛的碳元素未被氧化成+4 价,___________。
(4)为研究红色固体产物的组成,进行如下实验(以下每步均充分反应):
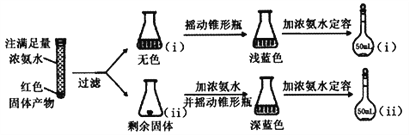
已知:Cu2O ![]() [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色)![]() [Cu(NH3)4]2+(蓝色)
[Cu(NH3)4]2+(蓝色)
①摇动锥形瓶i的目的是__________。
②锥形瓶ii中固体完全溶解得深蓝色溶液的离子方程式为_______________。
③将容量瓶ii中的溶液稀释100倍后,溶液的颜色与容量瓶i相近。由此可知固体产物的组成及物质的量之比约为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 2.8 g环已烷含共价键数目为0.4NA
B. 过氧化钠与水反应,生成0.1 mol氧气时,转移的电子数为0.4NA
C. 142 g Na2SO4和Na2HPO4固体混合物中,阴阳离子总数为3NA
D. 用惰性电极电解CuSO4溶液后,如果加入0.1 molCu(OH)2能使溶液复原,则电路中转移电子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com