
 铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:
铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:分析 (1)钢铁在潮湿的空气中发生吸氧腐蚀,正极上得电子发生还原反应;铁和铁离子能发生氧化还原反应生成亚铁离子;
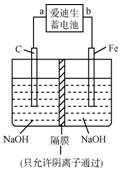
(2)①放电时,铁棒作负极,碳棒作正极,据此判断a的电极;失电子的物质发生氧化反应;
②铁失电子和氢氧根离子生成高铁酸根离子和水;
③高铁酸根离子有强氧化性,被还原生成的三价铁离子能发生生成胶体,胶体具有吸附性.
解答 解:(1)钢铁在潮湿的空气中发生吸氧腐蚀,正极上氧气得电子和水反应生成氢氧根离子O2+4e-+2H2O=4OH-;铁和铁离子能发生氧化还原反应生成亚铁离子,离子方程式为:2Fe3++Fe=3Fe2+,导致溶液中不存在铁离子;
故答案为:O2+4e-+2H2O=4OH-;2Fe3++Fe=3Fe2+;
(2)①放电时,铁作负极,碳棒作正极,所以放电时a是负极,b是正极;充电时,氢氧化镍失电子生成氧化镍,发生氧化反应;
故答案为:a;氧化反应;
②阳极上铁失电子和氢氧根离子反应生成高铁酸根离子和水,离子方程式为:Fe-6e-+8OH-=FeO42-+4H2O;
故答案为:Fe-6e-+8OH-=FeO42-+4H2O;
③高铁酸钠具有强氧化性,所以能杀菌消毒;高铁酸钠能被还原生成铁离子,铁离子能水解生成氢氧化铁胶体,胶体具有吸附性,能吸附悬浮杂质,所以能净水;
故选BC.
点评 本题以安迪生电池为载体考查了原电池原电池和电解池原理,难度不大,明确高铁酸钠能作为一种新型净水剂的原理.


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | Fe在一定条件下可与浓盐酸、稀硫酸、浓硝酸等剧烈反应 | |
| B. | Al、Cl2均能和NaOH溶液发生氧化还原反应,且两单质的作用不相同 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解,若再继续加入KNO3固体,铜粉会溶解 | |
| D. | 金属单质Na、Mg、Fe在一定条件下与水反应都生成H2和相应的碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
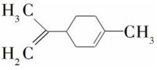
| A. | 柠檬烯的一氯代物有7种 | |
| B. | 柠檬烯和丁基苯互为同分异构体 | |
| C. | 柠檬烯的分子中所有的碳原子可能在同一个平面上 | |
| D. | 在一定条件下,柠檬烯可以发生加成、取代、氧化、还原等反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 次氯酸的电子式: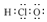 | B. | S2-的结构示意图: | ||
| C. | O-18的原子符号:${\;}_{\;}^{15}$O | D. | CO2分子的结构式:O=C=O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY | B. | XY2 | C. | XY3 | D. | XY4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素A、B组成的化合物常温下一定呈气体 | |
| B. | 元素C、D的最高价氧化物对应的水化物之间不能发生反应 | |
| C. | 元素B的单质可被热的浓硫酸或浓硝酸氧化 | |
| D. | 化合物AE与CE含有相同类型的化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ②③④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ①③⑤ | C. | ②③④ | D. | ①⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com