
| A. | 在放电时,正极发生的反应是Pb(s)+SO42-(ag)-2e-═PbSO4(s) | |
| B. | 在充电时,电池中硫酸的浓度不断变小 | |
| C. | 在充电时,阴极发生的反应是PbSO4(s)+2e-═Pb(s)+SO42-(ag) | |
| D. | 在放电时,该电池的负极材料是氧化铅 |
分析 A.原电池正极上得电子发生还原反应;
B.根据电池反应式确定硫酸浓度是否变化;
C.充电时,负极与阴极相连得电子发生还原反应;
D.在放电时,该电池的负极材料是铅.
解答 解:A.蓄电池放电时,正极上二氧化铅得电子发生还原反应,反应式为PbO2+4H++SO42-+2e-═PbSO4+2H2O,故A错误;
B.根据电池反应式知,放电时消耗硫酸,所以硫酸浓度降低,故B错误;
C.充电时,负极与阴极相连,则阴极的电极反应为PbSO4+2e-=Pb+SO42-,故C正确;
D.在放电时,该电池的负极材料是铅,故D错误;
故选C.
点评 本题考查铅蓄电池,注意原电池和电解池的分析,明确工作原理及电子守恒是解答本题的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
 一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )
一定温度下,两个体积相等的连通容器用活塞分开,左右两室各充入一定量NO和O2,恰好使两容器内气体密度相同,打开活塞,充分混合反应.下列判断正确的是(不考虑NO2转化为N2O4)( )| A. | 最终容器内无O2存在 | B. | 反应前、后左室气体压强不变 | ||
| C. | 反应前、后右室气体密度不变 | D. | 开始时左右两室气体分子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水或酸性KMnO4溶液鉴别甲烷和乙烯 | |
| B. | 向酒精中加入足量生石灰检验酒精中是否含有少量水 | |
| C. | 在盛有2mL无水乙醇的试管中放入绕成螺旋状的光洁铜丝,加热可制得乙醛 | |
| D. | 将裂解气通入到酸性KMnO4溶液中来证明裂解气中是否有乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
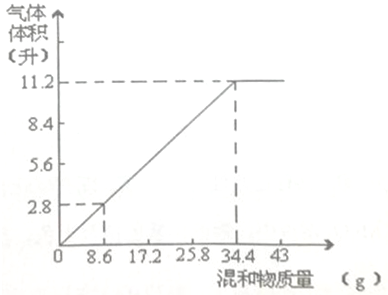 加热碳酸铵[(NH4)2CO3】并使产物全部变成气态.
加热碳酸铵[(NH4)2CO3】并使产物全部变成气态.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向盐酸和AlCl3的混合溶液中逐滴加入NaOH溶液至过量,生成沉淀Al(OH)3的量随着加入NaOH溶液体积的变化关系如图所示,下列说法正确的是
向盐酸和AlCl3的混合溶液中逐滴加入NaOH溶液至过量,生成沉淀Al(OH)3的量随着加入NaOH溶液体积的变化关系如图所示,下列说法正确的是| A. | 在a点对应的溶液中,加入Mg2+、I-、NH4+、NO3-离子仍能大量共存 | |
| B. | 图中B→C的过程中,实际发生的离子方程式为Al(OH)3+OH-=AlO2-+2H2O | |
| C. | 若b、c的纵坐标数值相同,则横坐标数值之比为1:3 | |
| D. | 原溶液中盐酸和AlCl3物质的量的浓度之比为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2~4 s内的平均反应速率为0.2 mol•L-1•s-1 | |
| B. | 前4 s内的平均反应速率为0.3 mol•L-1•s-1 | |
| C. | 前2 s内的平均反应速率为0.4 mol•L-1•s-1 | |
| D. | 2 s末的反应速率为0.4 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其他条件不变时,增大反应的物质的量,反应速率增大,化学平衡发生移动 | |
| B. | 其他条件不变时,升高温度,化学平衡向放热反应的方向移动 | |
| C. | 其他条件不变时,增大压强,化学反应速率增大,化学平衡发生移动 | |
| D. | 其他条件不变时,使用催化剂,化学反应速率改变,化学平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,其分子式是C9H10O3,含氧官能团的名称是:羧基、醇羟基.
,其分子式是C9H10O3,含氧官能团的名称是:羧基、醇羟基.
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯. | D装置中:溶液变红 E装置中:水层溶液变黄,振荡后,CCl4层无明显变化,持续通入一段时间后,CCl4层变为棕色 | ⑨单质、Br2、Fe3+的氧化性由强到弱的顺序是: ⑨单质(或Cl2)>Br2>Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com