
为了测定铜铁合金中铜的质量分数,在10.00g试样中加入200mL、0.6mol/L的稀硝酸,充分反应后剩余金属7.48g,再向其中加入50mL、0.4mol/L的稀硫酸,充分振荡后剩余金属6.60g。若硝酸的还原产物只有NO,下列说法正确的是
| A.上述测定不能达到实验目的 | B.剩余的7.48g金属为铜 |
| C.共生成NO气体 0.04mol | D.该合金中铜的质量分数为69.2% |
CD
解析试题分析:铁的金属性强于铜的,所以硝酸首先氧化金属铁,第一次反应后金属过量,硝酸不足,说明生成物一定有硝酸亚铁。加入稀硫酸后金属又溶解了7.48g-6.60g=0.88g,硫酸中氢离子的物质的量是0.05L×0.4mol/L×2=0.04mol,则根据方程式3M+2NO3-+8H+=3M2++2NO↑+4H2O可知,NO的物质的量是0.01mol,参加反应的金属的物质的量是(0.04mol÷8)×3=0.015mol,则M的相对原子质量是0.88÷0.015=58.67,这说明溶解的金属是铁和铜,所以剩余的7.84g金属是铁和铜的混合物,因此第一次溶解的金属铁是10.00g-7.48g=2.52g,物质的量是2.52g÷56g/mol=0.045mol,6.60g全部是金属铜。硝酸的物质的量是0.2L×0.6mol/L=0.12mol,根据方程式3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O可知,生成物硝酸亚铁的物质的量是0.045mol,NO的物质的量是0.03mol,因此共放出NO是0.04mol。设第二次消耗金属铁和铜的物质的量分别是x和y,则56x+64y=0.88、2x+2y=0.01×3,解得x=0.01mol、y=0.005mol,所以合金中铜的质量是6.60g+0.005mol×64g/mol=6.92g,所以该合金中铜的质量分数为69.2%,答案选CD。
考点:考查铁、铜与硝酸以及硫酸反应的有关计算。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:单选题
将6.85g Fe和Al的混合物溶于200mL 浓度为C mol/L的HNO3溶液中,得到标准状况下的NO、N2O混合气体共3.36L,测得反应后溶液的pH为0,再向所得溶液中加入过量NaOH溶液充分反应后生成沉淀质量为5.35 g。若不考虑反应前后溶液体积变化,则下列有关判断正确的是( )。
| A.Fe与Al 的物质的量之比为1:1 |
| B.混合气体中NO为0.03mol ,N2O为0.12mol |
| C.原HNO3溶液的浓度C=4.9mol/L |
| D.反应中被还原的HNO3为0.15mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氮化铝(化学式为AlN,其中Al为+3价)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN 可通过反应:Al2O3+N2+3C 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
| A.Al2O3是氧化剂 | B.N2被氧化 |
| C.AlN的摩尔质量为41 g | D.生成1 mol AlN转移3 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于反应CaO + 3C→CaC2 + CO,下面哪种表述能最好地说明该反应是一个氧化还原反应
| A.CaO失氧变为CaC2 |
| B.碳元素失去了电子,同时也得到了电子 |
| C.钙元素的化合价在反应前后发生了改变 |
| D.单质碳的状态发生了变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据表中信息判断,下列选项不正确的是
| 序号 | 反应物 | 产物 |
| ① | KMnO4 、H2O2 、H2SO4 | K2SO4 、MnSO4 ...... |
| ② | Cl2 、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4- ...... | Cl2 、Mn2+ ...... |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知OCN-中每种元素原子都满足8电子稳定结构,反应OCN-+OH-+C12→CO2+N2+C1-+H2O(未配平)中,如果有9 mol C12完全反应,则被氧化的OCN-的物质的量为
| A.2mol | B.3mol | C.4mol | D.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
0.02 mol FeS2与一定浓度的硝酸完全反应,Fe元素和S元素全部转化为 和
和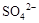 ,同
,同
时产生氮的氧化物(NO、NO2、N2O4)混合气体共0.25 mol,该混合气体的平均相对分子质量可能是
| A.30 | B.46 | C.50 | D.66 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
水热法制备纳米颗粒Y(化合物)的反应为
3Fe2++2S2O32-+O2+aOH-=Y+S4O62-+2H2O,下列说法中不正确的是
| A.a=4 |
| B.Y的化学式为Fe2O3 |
| C.S2O32-是还原剂 |
| D.每有1 mol O2参加反应,转移的电子总数为4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在下列变化中,按氮元素被还原、被氧化、既被氧化又被还原、既不被氧化又不被还原的顺序排列正确的是 ①大气通过闪电固氮 ②硝酸分解 ③实验室用氯化铵和消石制取氨气 ④二氧化氮溶于水中
| A.①②③④ | B.②④①③ | C.①③④② | D.②①④③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com