
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,2.24 L CCl4中含Cl原子数目为0.4NA
B. 白磷分子(P4)呈正四面体结构,12.4 g白磷中含有P-P键数目为0.6NA
C. 5.6 g铁粉在2. 24 L(标准状况)氯气中充分燃烧,失去的电子数为0.3NA
D. 常温常压下,10 g46%酒精水溶液中含氧原子总数为0.1NA
科目:高中化学 来源: 题型:
【题目】以淀粉为基本原料可制备许多物质,如:
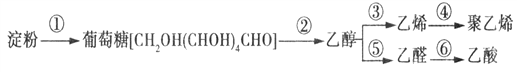
下列有关说法中正确的是( )
A. 淀粉是糖类物质,有甜味,与纤维素互为同分异构体
B. 反应③是消去反应、反应④是加聚反应、反应⑤是取代反应
C. 乙烯、聚乙烯分子中均含有碳碳双键,均可被酸性KMnO4溶液氧化
D. 在加热条件下,可用银氨溶液将鉴别葡萄糖和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
A.1:4
B.1:5
C.2:3
D.2:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水溶液中H+和OH-的浓度变化曲线如图,下列说法正确的是( )
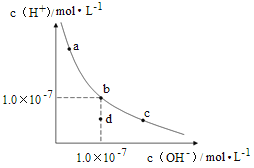
A. 升高温度,可能引起由c向b的变化
B. 该温度下,水的离子积常数为1.0×10-13
C. 该温度下,加入FeCl3可能引起由b向a的变化
D. 该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一分子式为C8H14N2O3的二肽,经水解后得到丙氨酸CH3CH(NH2)COOH和另一种氨基酸R,则R的分子式为( )
A.C5H9NO
B.C5H9NO2
C.C5H9NO3
D.C5H9NO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol·L-1,c(SO42-)=0.8mol·L-1,则c(K+)为
A. 0.15 mol·L-1 B. 0.2 mol·L-1 C. 0.3 mol·L-1 D. 0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯和甲苯的说法正确的是
A. 甲苯苯环上的一个氢原子被-C3H7取代得到的有机物结构共有3种
B. 等质量的苯和甲苯分别完全燃烧后,生成的CO2与消耗的O2的物质的量均相同
C. 苯的二溴代物有三种,则四溴代物有三种
D. 间二甲苯只有一种结构可说明苯分子中不存在碳碳单键与碳碳双键交替的结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如图所示。请回答下列问题:

(1)Cu元素基态原子的外围电子排布式为________。
(2)元素C、N、O的第一电离能由大到小的顺序为________。
(3)配合物A中碳原子的轨道杂化类型为________。
(4)1 mol氨基乙酸钠(H2NCH2COONa)含有σ键的数目为________________。
(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体:________(写化学式)。
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图。则该化合物的化学式是________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释物质用途或现象的方程式不正确的是( )
A. 铝热反应用于焊接钢轨:2Al+Fe2O3![]() Al2O3+2Fe
Al2O3+2Fe
B. 汽车尾气中发生的催化转化反应:2NO+2CO![]() N2+2CO2
N2+2CO2
C. 燃煤时加入石灰石减少SO2的排放:2CaCO3+2SO2+O2![]() 2CaSO3+2CO2
2CaSO3+2CO2
D. 用Na2CO3溶液处理水垢中的不溶物CaSO4:CaSO4+ CO32-![]() CaCO3+ SO42-
CaCO3+ SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com