
分析 在此溶液中加入过量盐酸,产生气泡,溶液颜色变深,但仍澄清,则一定不含SiO32-,溶液颜色变深,一定是生成了碘单质,一定含有I-、NO3-,并且原溶液中的阴离子种类减少了3种,据此确定另一种离子是亚硫酸根离子,亚硫酸根离子具有还原性,能被硝酸氧化为硫酸根离子,以此来解答.
解答 解:在此溶液中加入过量盐酸,产生气泡,溶液颜色变深,但仍澄清,则一定不含SiO32-,溶液颜色变深,一定是生成了碘单质,一定含有I-、NO3-,并且原溶液中的阴离子种类减少了3种,亚硫酸根离子具有还原性,根据6I-+8H++2NO3-=3I2+2NO↑+4H2O、3SO32-+2H++2NO3-=3SO42-+2NO↑+H2O知道,一定含有亚硫酸根离子,可能含有硫酸根离子.
(1)在此溶液中加入过量盐酸,仍澄清,则一定不含SiO32-,因为SiO32-+2H+=H2SiO3↓,硅酸是白色沉淀,硅酸钠溶液俗称水玻璃,硅酸钠溶液与足量氯化铵溶液反应的离子方程式为SiO32-+2NH4+=H2SiO3↓+2NH3↑,
故答案为:没有;水玻璃;SiO32-+2NH4+=H2SiO3↓+2NH3↑;
(2)根据6I-+8H++2NO3-=3I2+2NO↑+4H2O、3SO32-+2H++2NO3-=3SO42-+2NO↑+H2O知道生成的气体中一定有NO,是一种无色无味、难溶于水的有毒气体,属于大气污染物,是不成盐氧化物,不能被NaOH溶液吸收,
故答案为:NO;ACD;
(3)根据6I-+8H++2NO3-=3I2+2NO↑+4H2O、3SO32-+2H++2NO3-=3SO42-+2NO↑+H2O知道,加入盐酸溶液中减少的3种离子是SO32-、I-、NO3-,
故答案为:SO32-、I-、NO3-;6I-+8H++2NO3-=3I2+2NO↑+4H2O;3SO32-+2H++2NO3-=3SO42-+2NO↑+H2O;
(4)原溶液中可能含有的阴离子是SO42-,故答案为:SO42-.
点评 本题考查常见离子的检验,为高频考点,把握离子的性质、发生的反应为解答的关键,侧重分析与实验能力的考查,注意发生的氧化还原反应,题目难度不大.


科目:高中化学 来源: 题型:实验题
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | CO | H2 | |||
| 1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 0.5 | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 营养液所含成分 | 质量(g) |
| KCl | a |
| K2SO | b |
| NH4Cl | 428 |
| A. | 53.5 和214 | B. | 74.5 和348 | C. | 74.5 和696 | D. | 149 和696 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:填空题
某金属加工厂排放的污水中含有CuSO4、ZnSO4、FeSO4,某研究小组利用该污水回收工业重要原料硫酸锌和有关金属,其流程如右图所示:请回答下列问题:
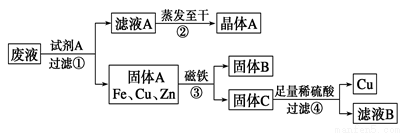
(1)下列说法正确的是________。
A.该工艺流程中发生了3个置换反应
B.CuSO4与MgCl2可以发生复分解反应
C.步骤①②③④都包含化学变化
D.滤液A和滤液B含有相同的溶质
(2)写出步骤①发生反应的离子方程式:_______________、________________。
(3)步骤④中加入足量稀硫酸的目的是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com