
| A. | 12C和14C | B. | O2与O3 | ||
| C. | 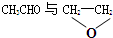 | D. | CH3CH2CH2CH3与CH3CH2CH2CH2CH3 |
分析 具有相同分子式而结构不同的化合物互为同分异构体;
具有相同质子数,不同中子数的同一元素的不同核素互为同位素;
结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物;
相同元素组成,不同形态的单质互为同素异形体,根据以上概念进行判断.
解答 解:A.12C和14C是质子数相同中子数不同的同一元素,互称同位素,不是同分异构体,故A错误;
B.O2与O3是氧元素的不同单质,互称同素异形体,不是同分异构体,故B错误;
C.CH3CHO与 的分子式相同、结构不同,互为同分异构体,故C正确;
的分子式相同、结构不同,互为同分异构体,故C正确;
D.CH3CH2CH2CH3与CH3CH2CH2CH2CH3都是烷烃,结构相似,在分子组成上相差1个CH2,互为同系物,故D错误;
故选C.
点评 本题考查了同分异构体的判断,题目难度不大,掌握同分异构体、同系物、同位素等的概念及实质是解题关键,试题培养了学生的灵活运用能力.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 现象 | 结论 | |
| A | 淀粉溶液中加入碘水 | 溶液变蓝 | 说明淀粉没有水解 |
| B | 将乙醇与酸性重铬酸钾(K2Cr2O7)溶液混合 | 橙色溶液变为绿色 | 乙醇具有还原性 |
| C | 蔗糖溶液中加入稀硫酸,水解后加入新制的Cu(OH)2悬浊液,加热 | 未出现砖红色沉淀 | 水解的产物为非还原性糖 |
| D | 将新制Cu(OH)2与葡萄糖溶液混合加热 | 产生砖红色沉淀 (Cu2O) | 葡萄糖具有氧化性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
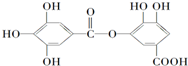
| A. | 在一定条件下,1 mol该物质最多能与6 mol NaOH完全反应 | |
| B. | 有弱酸性,1 mol该有机物与溴水反应,最多能消耗4 mol Br2 | |
| C. | 在Ni催化下,1 mol该物质可以和7 mol H2发生加成反应 | |
| D. | 它能发生水解反应,水解后只能生成两种产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打与盐酸反应 CO32-+2H+═H2O+CO2↑ | |
| B. | 向烧碱溶液中通入过量的CO2 CO2+2OH-═CO32-+H2O | |
| C. | 小粒钠投入冷水中 2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 用稀硝酸洗涤试管内壁的银镜:Ag+4H++3NO3-═Ag++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com