
分析 (1)沙子不溶于水;
(2)硝酸钾和氯化钠的溶解度受温度影响不同;
(3)水和汽油分层;
(4)二者互溶,但沸点不同;
(5)碘不易溶于水,易溶于有机溶剂.
解答 解:(1)沙子不溶于水,则选择过滤法分离,故答案为:E;
(2)硝酸钾和氯化钠的溶解度受温度影响不同,则选择结晶法分离,故答案为:C;
(3)水和汽油分层,则选择分液法分离,故答案为:D;
(4)二者互溶,但沸点不同,则选择蒸馏法分离,故答案为:F;
(5)碘不易溶于水,易溶于有机溶剂,则选择有机溶剂进行萃取、分液,然后蒸馏得到碘,故答案为:AF.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意分离原理的理解,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 最高价氧化物水化物的碱性:Y<Z | B. | 简单气态氢化物的热稳定性:X<W | ||
| C. | 简单离子的半径:Y<X | D. | X分别与Z、W形成化合物的熔点:Z<W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③ | C. | ②③ | D. | 只有③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
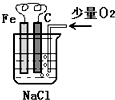 分析图,按要求写出有关反应方程式:
分析图,按要求写出有关反应方程式:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| CaSO4 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广燃煤脱硫技术,减少SO2污染,同时把煤粉碎了再燃烧以提高煤的燃烧效率 | |
| B. | 开发太阳能、风能和氢能等能源代替化石燃料,有利于节约资源、保护环境 | |
| C. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 | |
| D. | 在汽车尾气处理器中使用新的催化剂,促使平衡2CO+2NO?2CO2+N2向正反应方向移动,减少污染物的排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 黄铁矿的主要成分是FeS | B. | SO3与水反应是放热反应 | ||
| C. | 用98.3%的硫酸吸收SO3 | D. | 热交换的目的是充分利用反应热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com