
下列物质中,按只有氧化性、只有还原性、既有氧化性又有还原性的顺序排列的一组是 ( )
A.F2、K、HCl B.Cl2、Al、H2 C.NO2、Na、Fe2+ D.Mg2+、SO2、H2O
科目:高中化学 来源: 题型:
已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且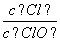 的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )
的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )
A.若某温度下,反应后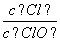 =11,则溶液中
=11,则溶液中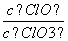 =
=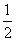
B.参加反应的氯气的物质的量等于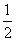 a mol
a mol
C.改变温度,反应中转移电子的物质的量ne的范围: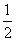 a mol≤ne≤
a mol≤ne≤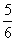 a mol
a mol
D.改变温度,产物中KClO3的最大理论产量为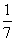 a mol
a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
正丁醚常用作有机反应的溶剂。实验室制备正丁醚的主要实验装置如右图:
反应物和产物的相关数据如下
| 相对分子质量 | 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
| 正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
| 正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
合成正丁醚的步骤:
①将6 mL浓硫酸和37 g正丁醇,按一定顺序添加到A中,并加几粒沸石。
②加热A中反应液,迅速升温至135℃,维持反应一段时间。分离提纯:
③待A中液体冷却后将其缓慢倒入盛有70 mL水的分液漏斗中,振摇后静置,分液得粗产物。
④粗产物依次用40 mL水、20 mL NaOH溶液和40 mL水洗涤,分液后加入约3 g无水氯化钙颗粒,静置一段时间后弃去氯化钙。
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g。
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为______________________________。
写出步骤②中制备正丁醚的化学方程式______________________________。
(2)加热A前,需先从__________(填“a”或“b”)口向B中通入水。
(3)步骤③的目的是初步洗去 ,振摇后静置,粗产物应从分液漏斗的  (填“上”或“下”)口分离出。
(填“上”或“下”)口分离出。
(4)步骤④中最后一次水洗的目的为______________________________。
(5)步骤⑤中,加热蒸馏时应收集__________(填选项字母)左右的馏分。
a.100℃ b. 117℃ c. 135℃ d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A。分水器中上层液体的主要成分为__________,下层液体的主要成分为__________。(填物质名称)
(7)本实验中,正丁醚的产率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
完成下列化学方程式的配平
⑴ H2S + HNO3 ── H2SO4 + NO2 + H2O
⑵ C + H2SO4 ── SO2↑ + CO2↑ + H2O
⑶ Zn + HNO3 ── Zn(NO3)2 + NH4NO3 + H2O
⑷ NaClO3 + FeSO4 + H2SO4 ── NaCl + Fe2(SO4)3 + H2O
⑸ Fe(OH)2+ O2+ H2O── Fe(OH)3
⑹ KClO3+ HCl(浓)- KCl+ ClO2+ Cl2+ H2O
⑺ KMnO4 + HCl── KCl + MnCl2 + Cl2↑ + H2O
⑻ Fe(NO3)3+ NaOH+ Cl2── Na2FeO4+ NaNO3+ NaCl+ H2O
⑼ P + KOH + H2O── KH2PO4 + PH3↑
⑽ KCl+ KClO3+ H2SO4── K2SO4+ Cl2↑+ H2O
⑾ FeS2+ O2 - Fe2O3+ SO2
⑿ H2C2O4+ KMnO4+ H2SO4── CO2+ K2SO4+ MnSO4+ H2O
⒀ MnO2+ H++ Cl-── Mn2++ Cl2↑+ H2O
⒁ Cu+ H++ NO3-── Cu2++ NO↑+ H2O
⒂ NO3—+ Zn+ OH—+ H2O── NH3+ Zn(OH)42-
查看答案和解析>>
科目:高中化学 来源: 题型:
某物质中元素被氧化,则该元素一定是 ( )
①化合价升高;②化合价降低;③得到电子或电子对偏向;④失去电子或电子对偏离
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下述三个实验均能发生化学反应:
| 实验① | 实验② | 实验③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铜丝放入氯化铁溶液中 |
下列判断中正确的是( )
A.实验①中铁钉只作还原剂 B.实验②中Fe2+既显氧化性又显还原性
C.实验③中发生置换反应 D.上述实验证明氧化性:Fe3+>Fe2+>Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
配平下列氧化还原反应方程式,并标明反应④电子转移的方向和数目。
① H2S+
H2S+ H2SO3——
H2SO3—— S↓+
S↓+ H2O
H2O
氧化产物是_________,还原产物是__________,二者质量比是________。
② Cl2+
Cl2+ KOH——
KOH—— KCl+
KCl+ KClO3+
KClO3+ H2O
H2O
氧化剂是________,还原剂是________,二者物质的量之比是__________。
③ KClO3+
KClO3+ HCl——
HCl—— KCl+
KCl+ Cl2↑+
Cl2↑+ H2O
H2O
HCl的作用是________,被还原的元素是__________,当反应过程中有3 mol电子转移时,可产生氯气________mol。
④ KIx+
KIx+ Cl2+
Cl2+ H2O——
H2O—— KCl+
KCl+ HIO3+
HIO3+ HCl
HCl
若KIx与Cl2的化学计量数之比为1∶8,则x=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实中,不能用勒·夏特列原理解释的是( )
A.在溴水中存在如下平衡:Br2+H2O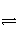
 HBr+HBrO,当加入NaOH溶液后颜色变浅
HBr+HBrO,当加入NaOH溶液后颜色变浅
B.对2H2O2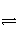
 2H2O+O2的反应,使用MnO2可加快制O2的反应速率
2H2O+O2的反应,使用MnO2可加快制O2的反应速率
C.反应CO+NO2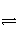
 CO2+NO ΔH<0,升高温度使平衡向逆反应方向移动
CO2+NO ΔH<0,升高温度使平衡向逆反应方向移动
D.合成氨反应:N2+3H2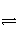
 2NH3 ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施
2NH3 ΔH<0,为使氨的产率提高,理论上应采取低温高压的措施
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com